хирургическое лечение, описание способов операций
Оперативное вмешательство — не самая крайняя мера при лечении болезней органов пищеварения. Зачастую, это вынужденная необходимость, которая обусловлена многими факторами и показателями. А в случае с ГЭРБ, хирургическое лечение может стать основным приемлемым методом избавления от выраженных загрудинных болей и невыносимой изжоги.
Решение о проведении операции принимают не только врачи-хирурги, но и терапевты, а так же и гастроэнтерологи, поэтому любое вмешательство серьезно взвешено и всегда оправдано.
Виды операций при лечении ГЭРБ
Условно хирургические операции, проводимые для лечения гастроэзофагеальной рефлюксной болезни, можно разделить на два типа.
- Операция для лечения непосредственных причин ГЭРБ.
- Устранение последствий или осложнений, которые развились в результате неправильного или несвоевременного лечения.
Первый вид оперативного лечения проводят в плановом порядке. Второй вид нередко проводится экстренно, к примеру, в результате открывшегося массивного кровотечения.
Показания к проведению операции при ГЭРБ
В каких случаях стоит прибегнуть именно к оперативному виду лечения.
- Об операциях идет речь, когда длительные курсы лекарственных веществ в максимальных дозах не приносят облегчения человеку, страдающему этим неприятным недугом.
- Агрессивное молниеносное течение ГЭРБ тоже показание к операции. Когда количество рефлюксов (забросы кислоты или другого желудочного содержимого в пищевод) ежедневно превышает 50 и более, боли не купируются препаратами, изжога беспокоит постоянно не зависимо от приема пищи, а при исследовании выявляется эзофагит 5 степени.
- Грыжа пищеводного отверстия диафрагмы при сочетании с гастроэзофагеальной рефлюксной болезнью тоже исправляется хирургическим методом.
- Любое осложнение — это показание к операции: пищеводное кровотечение, пищевод Барретта, множественные язвы и значительное сужение органа — стриктуры.
- Относительное показание к оперативному лечению — это отсутствие денег для длительной терапии. Курсы лечения могут затянуться от двух-трех месяцев, как в случае с эзофагитом 3 и 4 степени тяжести, до года и более, что характерно для пищевода Барретта. При этом необходимо постоянно использовать блокаторы протонного насоса, курсами антациды (альгинаты) и прокинетики. И это в лучшем случае, иногда терапия сочетает препараты пяти групп и более. Не всегда бюджет человека выдерживает такие траты.
- Тяжелые аллергические реакции на все группы препаратов против ГЭРБ.
Противопоказания
Оперативное лечение не всегда показано, есть случаи в которых его применять не имеет смысла.
- При наличии тяжелой сопутствующей патологии: нарушение ритма сердца, почечная недостаточность.
- Преклонный возраст.
Способы хирургического лечения ГЭРБ
Одной из ведущих причин развития болезни является несостоятельность нижнего пищеводного сфинктера (это та мышца, которая не дает проходить пище обратно из желудка вверх). В результате чего, желудочное содержимое постоянно попадает в пищевод — получаются рефлюксы, что чувствуется в виде изжоги и боли за грудиной.
Чтобы убрать эти симптомы нужно основательно укрепить мышцу. Существует несколько способов.
- Одна из самых распространенных операций при ГЭРБ — это фундопликация. Суть такого метода укрепления сфинктера заключается в подшивании части желудка к пищеводу (в процессе самой операции желудок подтягивают кверху, им окутывают нижнюю часть трубки пищевода). Есть несколько видов таких операций, которые называются по имени автора, ее придумавшего (самая часто применяемая на сегодня — фундопликация по Ниссену).
- Еще один вариант — эндоскопическая коррекция сфинктера (через зонд).
На что только не отваживались хирурги при коррекции сфинктера — были попытки наложения шва на мышцу с целью ее укрепления, врачи даже пытались ввести силикон в сфинктер. Все это дополнительно сопровождалось физиотерапевтическим воздействием на пищевод изнутри. Но пока такое лечение не принесло видимых результатов.
Зависимость способа операции от осложнений ГЭРБ
Вид и способ хирургического лечения, зависит от полученных осложнений гастроэзофагеальной рефлюксной болезни.
- Множественные язвы длительно лечат поочередно в условиях стационара и амбулаторно. Если они не заживают и начинают обильно кровоточить в результате поражения сосудов, то такие дефекты ушивают.
- Стриктуры (сужения пищевода в результате замещения рубцовой тканью) стараются устранить, так как просвет органа значительно сужается. Для этого их «вырезают», восстанавливая естественную проходимость пищевода.
- Пищевод Барретта лечат двумя способами: лазерная коагуляция (прижигание) участков замещенного эпителия либо полное хирургическое удаление пораженной части пищевода.
Не стоит бояться оперативного лечения в случае с ГЭРБ. Это простые операции с небольшими разрезами и минимальными последствиями. Они помогают людям, страдающим этой малоприятной болезнью почувствовать свободу от вынужденного постоянного применения лекарств. Любое лечение важно тщательно взвесить.
Гастроэзофагиальная рефлюксная болезнь: новое эндоскопическое лечение
Полный текст статьи:
Опасения по отношению фармакотерапии
При наличии 2х таких эффективных вариантов лечения, персональные предпочтения и сомнения много значат в принятии решения. Хотя ингибиторы протонной помпы используются более 10 лет и кажутся одними из наиболее безопасных препаратов, некоторые пациенты продолжают беспокоится по поводу пожизненного приема медикаментов из-за потенциальной возможности неизвестных в настоящее время или трудно распознаваемых побочных эффектов. Исследователи-хирурги выдвинули теорию, что использование антацидных препаратов играет определенную роль в быстро растущей частоте встречаемости аденокарциномы пищевода. Они защищают хирургическое лечение как средство создания механического барьера против рефлюкса гастродуоденальных канцерогенов. В дополнение к этому, некоторые пациенты испытывают сложности забывая о необходимости постоянного приема медикаментов или имея проблемы с их стоимостью. У небольшой группы пациентов могут возникать неприятные побочные эффекты при применении ингибиторов протонной помпы.
Опасения по поводу хирургического лечения
Хирургическое вмешательство, с другой стороны, связанно с очень низким, но непосредственным, риском общей анестезии и прямых осложнений. Лапароскопическая техника уменьшила степень хирургической травмы и сократила время пребывание в госпитале, но риск полностью не элиминирован и все еще существует возможность длительного периода плохого самочувствия связанного с операцией у некоторых пациентов. Так же пациенты обеспокоены, что эффект от хирургического лечения не будет длительным и им в конце концов придется снова принимать медикаменты для контроля симптомов ГЭРБ. Это опасение подтверждается недавно опубликованными результатами продолжительного совместного исследования сравнивающего пациентов рандомизированных для получения медикаментозного или хирургического лечения. Через в среднем 10 лет наблюдения более половины пациентов хирургической группы возобновили прием антацидных препаратов [1].
Эндоскопическое лечение: новые возможности для ГЭРБ
Решение — Применить фармакологический или хирургический контроль ГЭРБ? — остается наиболее важным при избрании лечебного подхода, однако сейчас новые механические эндоскопические способы лечения дают дополнительные возможности. В идеале, эндоскопическое лечение может проводиться без общей анестезии в амбулаторных условиях. Если созданный механический барьер признается недостаточным или становится менее эффективным с течением времени, он, теоретически, мог быть бы легче создан вновь, чем в случае хирургического или лапароскопического вмешательства.Три различных вида эндоскопической терапии находится в стадии развития:
- Использование эндоскопической «швейной машины». При использовании этой техники швы укладываются в области кардии для создания внутренней складки и подавления рефлюкса. Устройство, используемое для выполнения этой процедуры одобрено United States Food and Drug Administration (FDA) в прошлом году.
- Использование радиочастотного тока для фокального повреждения мускульного слоя гастроэзофагиального соединения и кардии, что приводит к рубцеванию, которое дает механический и нейромускулярный эффекты, ведущие к уменьшению рефлюкса. Устройство, применяемое при этом методе, было так же одобрено FDA в прошлом году.
- Использование эндоскопического введения инертных материалов в гастроэзофагиальное соединение для создания большего антирефлюксного барьера.
Эти новые методы лечения были темами нескольких клинических симпозиумов и научных публикаций, представленных на Гастроэнтерологической недели 2001 в Атланте, Джорджия, Май 20-23. Эта статья обсуждает эти методики и их применение в клинических условиях.
Эндоскопическая гастропластика по поводу ГЭРБ
Доктор Paul Swain, из Royal London Hospital, Лондон, Англия, врач изобретший эндоскопическую швейную машинку, представил свой опыт использования коммерчески выпускаемого устройства (EndoCinch; Bard; Billerica, Massachusetts) созданного для выполнения антирефлюксной гастропластики [2]. Доктор Swain описал свои результаты лечения с использованием 9-мм эндоскопической швейной машинки у 142 пациентов. Его техника включала наложение швов ниже гастроэзофагиального соединения и соединение тканей четырьмя завязанными экстрокорпорально узлами. Линейная конфигурация швов использовалась для создания нового пищевода 1-2 см длиной. Процедура выполнялась на амбулаторных пациентах в состоянии седации и занимала в среднем 30 минут. Доктор Swain отметил, что время выполнения процедуры было дольше в более неопытных руках и так же подчеркнул, что надеться переделать устройство используя внешнюю трубку меньшего диаметра. На среднем этапе оценки эффективности процедуры (через 12 недель) было отмечено значительное улучшение согласно системы подсчета симптомов по Demeester, увеличение длинны и давления нижнего пищеводного сфинктера (НПС) и уменьшения степени заброса кислого содержимого желудка в пищевод. Большинство пациентов были удовлетворены своими результатами и уменьшили дозу приема ингибиторов протонной помпы. Однако были и осложнения, обычно незначительные, но включившие и одну перфорацию. Что наиболее впечатляло в этом исследовании это доступность длительного наблюдения у многих пациентов, показывающих, что улучшение в симптоматике и показателях рН сохранялись через 2-4 года — с наличием интактных швов у некоторых пациентов через 5 лет. Среднедлительные результаты были описаны как сравнимые с оперативной фундопликацией, но в отличие от которой данная методика легко повторима (при необходимости), обратима и не требует общей анестезии и госпитализации. Результаты у пациентов с хиатальной грыжей диаметром более 2 см и более тяжелым эзофагитом были хуже и эта группа была исключена из дальнейших исследований. По результатам недавно опубликованных мультицентровых исследований выполненных в США и включавших 68 пациентов с нетяжелым рефлюксом без или с незначительной грыжей отмечено значительное улучшение в симптомах изжоги и регургитации, а рН мониторинг показал уменьшения заброса кислоты в пищевод. Пациенты были рандомизированны на создание либо циркулярной, либо линейной складки, но существенного различия в результатах получено не было. Было отмечена одна перфорация при наложении швов пролеченная антибиотикотерапией [3]. Доктор Isaac Raijman из Хюстона, Техас, представил результаты другого проведенного с США мультицентрового исследования [4]. Исследовавшаяся группа состояла 88 пациентов включающая людей с большой хиатальной грыжой и пищеводом Баррета (2%). Несмотря на то, что пациенты с ожирением были исключены из исследования, средний вес пациентов составил 201 lb. Улучшение в симптоматике было достигнуто у 80-90% пациентов в сроках 6 месяцев и пациенты с более выраженными грыжами и пищеводом Баррета имели такой же ответ на коротких сроках наблюдения. Сравнение эндоскопической и лапароскопической фундопликации было описано доктором V. Velanovich из Henry Ford Hospital, Детройт, Мичиган [5]. Всего 27 пациентов пролеченных эндоскопической фундопликацией были сравнены с пациентами с лапароскопическими вмешательствами. Краткосрочные результаты показали сходное улучшение в симптоматике, но значительно больше лапароскопически пролеченных пациентов (96%) были удовлетворены результатами вмешательства, чем пациентов после эндоскопической терапии. (78%). Было предложено провести рандомизированные контролированные исследования.
Новые эндоскопические устройства для эндоскопической пликации
(от переводчика — пликация — уменьшение размеров полого органа посредством наложения присборенных швов на стенку).
Много новых устройств для эндоскопической пликации гастроэзофагиального соединения с целью лечения ГЭРБ разрабатывается настоящее время. Несмотря на то, что эти методы были применены на животных моделях, все они не имеют значительных перспектив у людей. Доктор Tamir Ben-Menachem из Henry Ford Hospital описал свою работу с новым методом завязывания швов наложенных устройством Bard EndoCinch [6]. Обычная процедура включает связывание двух нитей 4-6 узлами завязываемыми экстрокорпорально и проталкиваемыми вниз «толкателем узлов». Каждый узел требует интубации пищевода для завязывания узла и еще одной для обрезки нити. Однако новая методика заменяет узел 2 мм пластиковой пробкой и кольцом (якорь) и требует одной интубации. Доставляющее устройство проводящееся по рабочему каналу эндоскопа закрепляет якорь на концах шва близко к слизистой и обрезает концы нитки. Это исследование, выполненное на свиньях, показывает, что использование якоря дает такую же силу натяжения как нитки и уменьшает количество интубации и время выполнения процедуры. Доктор Ram Chuttani из Beth Israel Medical Center, Бостон, Массачусетс, сообщил о своем опыте использования нового эндоскопического пликатара «во всю толщу», созданного NDO Surgical Inc.; Mansfield, Massachusetts на лабораторных моделях и препаратах желудка человека [7,8]. Другое новое устройство выполняющее пероральную фундопликацию по Нисану было представлено доктором Rodney J. Mason из the University of Southern California, Лос-Анжелес [9]. Процедура включает инвагинацию и фиксацию гастроэзофагиального соединения, таким образом, создавая функциональный ниппельный клапан в нижней части пищевода сравнимый с эффектом фундопликации по Нисану. Устройство (созданное Boston Scientific/Microvasive, Natick, Massachusetts, and Eberhard Karls University, Tübingen, Германия) позволяет устанавливать биоабсорбируемые клипсы под эндоскопическим контролем. Были описаны первые результаты тестирования этого устройства на бабуинах, они кажутся многообещающими.
Радиочастотная абляция (Процедура Stretta)
Процедура Stretta подразумевает доставление тепловой радиочастотной энергии к мышце нижнего пищеводного сфинктера и кардии. Одобренный FDA к клиническому использованию более года назад этот метод широко использовался и тестировался в многоцентровых исследованиях. Доктор George Triadafilopoulos из Stanford University School of Medicine, Стэнфорд, Калифорния, который недавно опубликовал начальные результаты мультицентровых исследований [10], представил новые клинические данные по этой процедуре [11]. Радиочастотная энергия доставляется через специальное устройство(Curon Medical, Inc., Sunnyvale, California) состоящее из бужа (в настоящее время проводимого по проволочному проводнику), балона-корзинки и четырех игольчатых электродов помещенных вокруг баллона. Баллон надувается, и иглы вводятся в мышцу под контролем эндоскопического наблюдения. Установка подтверждается измерением импеданса тканей и затем на концы игл подается высокочастотный ток с одновременным остужением слизистой путем подачи воды. Инструмент поворачивается для создания дополнительных «очагов повреждения» на разных уровнях и обычно наноситься 12-15 групп таких очагов. Антирефлюксный эффект процедуры Stretta связан по крайней мере с двумя механизмами. Один механизм — «уплотнение» обработанной области, которое становиться менее чувствительной к эффектам растяжения желудка после еды и которое создает механический барьер для рефлюкса. Другой механизм — нарушения афферентных вагальных проводящих путей от кардии вовлеченных в механизм транзиторного расслабления нижнего эзофагиального сфинктера. Увеличение числа транзиторных расслабления нижнего эзофагиального сфинктера считается важным признаком ГЭРБ у некоторых пациентов, процедура Stretta уменьшает число транзиторных расслабления нижнего эзофагиального сфинктера у людей и животных [12]. Доктор William C.E. Tam из Royal Adelaide Hospital, Аделаида, Австралия представил результаты исследования 15 пациентов подвергшихся процедуре Stretta. Он сообщил о значительном снижении числа транзиторных расслаблении нижнего эзофагиального сфинктера, уменьшение воздействия кислоты на пищевод и улучшении качества жизни пациентов [13]. Доктор Kenneth J. Chang из University of California Irvine Medical Center, Орандж, Калифорния, описал свою работу посвященную ультразвуковому измерению толщины стенок и толщены мышцы в области НПС у свиней пролеченных процедурой Stretta. Его результаты показали, что мышца НПС после лечения была значительно толще по данным УЗИ. Данные УЗИ были подтверждены гистологическими измерениями. Наблюдаемое утолщение возможно снижает растяжимость этой области и может быть частью антирефлюксного барьера возникающего после радиочастотного лечения. Это так же указывает, что УЗИ может быть полезным для мониторинга эффекта Stretta [14]. Доктор Triadafilopoulos так же отметил, что общая длительность процедуры для метода Stretta составила в среднем 53 минуты. Уровень серьезных осложнений составил 0,8% — было сообщено о 2 перфорациях и двух случаях аспирационной пневмонии развившейся через 1 неделю после лечения, обе из которых закончились смертью [11]. Уровень осложнений продолжает мониторироваться. Доктор Triadafilopoulos дополнительно сообщил о мультицентровом исследовании 119 пациентов с ГЭРБ. Все осложнения в этой серии были нетяжелые (всего = 8,4%). Наблюдалось значительное улучшение в симптомах ГЭРБ и качества жизни и уменьшения кислотного воздействия на пищевод и использование медикаментов. Улучшение в симптоматике сохранялось при 12 месячном наблюдении [11]. Доктор Heiko Pohl из Hitchcock Medical Center, Lebanon, Нью-Хенпшир, представил данные сравнивающие систему эндоскопического наложения швов Bard и процедуру Stretta в одном учреждении. Всего 20 пациентов было пролечено (BESS 13, Stretta 7), и результаты были близко эквивалентны со схожей продолжительностью процедуры, потребностью к седации и степенью клинического улучшения. Ни после одной из процедур серьезных осложнений не было [15].
Эндоскопические имплантанты
Имплантация инертных материалов в область нижнего пищеводного сфинктера выполнялась с общими неудовлетворительными результатами. Однако доступность новых материалов и их успешное применение в пластической хирургии и урологии привели к возобновлению интереса к этой терапии. Технически более легкая, чем сшивание и радиочастотная абляция, инъекция инертных материалов может так же титрироваться в зависимости от симптоматики при повторных введениях. Последние публикации об использовании подслизистого введения для этой цели микросфер Plexiglas (PMMA) говорят о хороших коротко срочных результатах и отсутствии серьезных осложнений [16]. Новые подходы к созданию механического барьера рефлюксу инъекцией инертных материалов в область гастроэзофагиального соединения было представлено доктором Jacques Deviere из Hospital Erasme, Брюссель, Бельгия на основе 15 больных с ГЭРБ. Пациенты получали инъекцию ethinyl-vinyl-alcohol (EVA) в мышцу кардии. Целью было — получить циркулярную диффузию материала, это было достигнуто у 10 из 15 пациентов и сопровождалось «сохранением» материала в области введения после инъекции. Увеличение давление НПС и улучшение симптоматики было отмечено у большинства пациентов при контроле через 4-12 месяцев [17]. Доктор David W. Easter из the University of California в Сан Диего представил данные мультицентрового исследования которое описывало имплантируемый эндоскопически гидрогеливые протезы. Исследование выполнялось на свиньях с использованием внешнего устройства и торокара для введения расширяющихся протезов в подслизистую в области НПС. Эта процедура оказалась безопасной и длительно эффективной при исследованиях на животной модели. Важно, что извлечение протеза с использованием эндоскопии оказалось возможным и технически простым. Исследования, касающиеся безопасности и функционального результата у людей сейчас проводятся [18].
Операция при ГЭРБ: показания, реабилитация, как проводится
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) нередко лечится оперативным путем. Применяется в плановом режиме по показаниям или экстренно при развитии тяжелых осложнений. Есть 2 техники хирургического вмешательства — фундопликация и эндоскопическая коррекция. Решение о проведении операции принимают не только хирурги, но и гастроэнтерологи и терапевты на основании результатов анализа и общего осмотра пациента.
3 основных показания
При разрыве пищевода возникает пневмоторакс — опасное осложнение ГЭРБ, воздух проходит плевральную полость и сразу сжимается легкое. Если не сделать вовремя операцию, есть опасность остаться инвалидом или даже умереть.
- Утяжеленные формы рефлюкса, что не поддается лечению консервативным путем: диетой, медикаментами.
- Молодость и отсутствие фоновых болезней. В этом случае хирургическое вмешательство избавляет от необходимости пожизненно принимать дорогостоящие препараты.
- Осложненный несостоятельностью антирефлюксной защиты вид ГЭРБ при сохранении активности пищевода.
Как проводится оперативное вмешательство?
Хирургическое лечение основано на укреплении сфинктерной мышцы. Проводится под общей анестезией. Предварительно проводится диагностика, отменить лекарства, что разжижают кровь. Перед операцией кушать легкую еду, но не пить и не есть после полуночи. Применяются 2 техники:
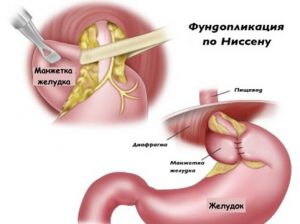 Коррекция дефекта сфинктера может быть проведена по методу Ниссена.
Коррекция дефекта сфинктера может быть проведена по методу Ниссена.- Фундопликация по Ниссену. Часть желудка подшивается к пищеводу.
- Эндоскопическая коррекция сфинктера (через зонд).
Положительные стороны хирургии:
- Устраняется причина появления рефлюкса, тогда как медикаменты устраняют лишь симптомы.
- В 90% случаев больные избавляются от основных признаков болезни.
- Только 14% прооперированных больных требуется дополнительный прием лекарств в связи с индивидуальными особенностями.
Вид операции выбираются в зависимости от тяжести ГЭРБ и наличия осложнений:
- Если в результате постоянных рефлюксов развились долго незаживающие язвы, их ушивают.
- Если имеются стриктуры (рубцовая ткань, что разрастаясь сужает пищевод), рассекают сложный участок электрохимическим методом и расширяют бужированием.
- При пищеводе Баретта применяют 2 методики: лазерное прижигание частиц замещенного эпителия или оперативное иссечение пораженных частей пищевода.
Послеоперационные трудности
- Инфекция, кровотечение.
- Трудности с глотанием, отрыжкой и рвотой.
- Повреждение органов (при обращении к неграмотным хирургам).
- Аллергия на анестезию.
- Малый риск рецидива, например, при появлении нового очага грыжи.
Противопоказания операции
 Пожилым пациентам такой способ лечения противопоказан.
Пожилым пациентам такой способ лечения противопоказан.- Пожилой возраст и плохое самочувствие пациента.
- Онкология.
- Обострение хронических патологий, в частности, сахарного диабета.
- Острые инфекции.
- Декомпенсированные недостаточности:
- сердечная;
- почечная;
- печеночная.
Вернуться к оглавлениюНе советуется делать операцию пациентам с сокращенным пищеводом, расстроенной моторикой.
Особенности реабилитации
После классической операции болезни ГЭРБ прооперированному пациенту снимают швы на 8-й день, но он 14 дней находится в стационаре под наблюдением врачей. Ему назначают полный покой, строгую диету и лекарства, предупреждающие воспаления, инфицирование, а также обезболивающие. После лапароскопии выписка происходит на 5-й день при отсутствии осложнений, а через месяц человек может приступать к работе, тогда как в первом случае потребуется 2 месяца на восстановление.
Весь реабилитационный период важно соблюдать некоторые правила:
 На этапе восстановления пациентам нельзя пить газировку.
На этапе восстановления пациентам нельзя пить газировку.- Принимать пищу маленькими частями.
- Не переедать, тщательно пережевывать.
- Во время еды держать прямо спину и полчаса после не ложиться в горизонтальное положение.
- Снизить количество или отказаться вовсе от дрожжевых, мучных, макаронных изделий, бобовых, лука и капусты.
- Не пить жидкости через соломинку, отказаться от газировки.
После любой операции в первые сутки пациент лежит, а со следующего дня начинает расхаживаться. Разрешено полужидкую диетическую пищу. Спустя некоторое время пищевые ограничения снимаются. Принимать можно только душ в течение первой недели. После омовения раны обрабатывают антисептиками (йодом, марганцовкой). Возвращение к обычному образу жизни, включая умеренные физнагрузки, питание, сексуальные отношения, возможны спустя месяц.
5.3. Хирургическое лечение гастроэзофагеальной рефлюксной болезни и ее осложнений
5.3.1.Показания к операции
В литературе существуют разноречивые мнения о показаниях к хирургическому лечению ГЭРБ. Часть хирургов ставят широкие показания к оперативной коррекции НЗФК, поскольку довольно часто через короткий промежуток времени после медикаментозного лечения наступает рецидив симптомов, а желудочно-пишеводный рефлюкс осложняется стенозом или рубцовой деформацией пищевода. Медикаментозное лечение у многих больных лишь отдаляет сроки развития осложнений, после чего оперативное вмешательство становится неотвратимым [27]. M.Meinero и соавт. [75] показанием к хирургическому лечению считают неэффективность консервативной терапии ГЭРБ в течение 6 месяцев независимо от наличия или отсутствия хиатальной грыжи, а также развитие осложнений — пептических язв или стеноза пищевода. А.Н.Дикушин [49] оперировал больных ГЭРБ вследствие грыжи пищеводного отверстия диафрагмы при неэффективности консервативной терапии в течение 4 недель, Г.А.Амбалов [54] — при наличии катарального рефлюкс-эзофагита с частыми обострениями, несоблюдение режима консервативного лечения (часто по экономическим соображениям), Richardson W.S. et al. [76] — снижении качества жизни. А.Ф.Черноусое и соавт. [77], Д.И.Тамулевичюте и соавт. [30], Redind von R. (1983) напротив, считали, что основная часть больных рефлюкс-эзофагитом нуждается в консервативном лечении. Оперативное вмешательство они применяли только при наличии строгих показаний: кровотечении, пептической стриктуре пищевода, подозрении на рак, гигантских грыжах пищеводного отверстия диафрагмы с анемическим синдромом, наличии сопутствующего заболевания, требующего хирургического лечения. В.Н.Васильев [78] полагал, что медикаментозная терапия у больных с тяжелым эрозивным эзофагитом предпочтительнее в сравнении с операцией. Menin R.A. и соавт. [70] предлагали ориентироваться не только на наличие рефлюкс-эзофагита, но и снижении давления в нижней пищеводной зоне высокого давления ниже 10 мм.рт.ст. и наличии интенсивного закисления пищевода.
Некоторые авторы считали оптимальным оперировать больных при «внепищеводных» проявлениях рефлюкс-эзофагита — повторные пневмонии, частое обострение хронического бронхита, хронический рефлюксный ларингит и фарингит, поражение зубов [26,79]. При оперативном вмешательстве по поводу хронической гастродуоденальной язве, сочетанной с ГЭРБ, необходимость коррекции кардии решается не однозначно. Согласно данным В.В.Вахидова и соавт. [80], К.И.Палтанавичюс [81] ГЭРБ у этих больных может развиться уже в ближайшие дни после ваготомии или резекции желудка. Целенаправленное рентгенологическое исследование позволило им выявить ГЭРБ у 35—49,1% больных после операций на желудке, не имевших клинических и рентгенологических признаков недостаточности кардии до вмешательства. Сотрудница нашей клиники Г.И.Климова [82] установила, что у 91,7% больных хронической язвой желудка и 12-перстной кишки, нуждающихся в оперативном лечении, имеется НЗФК вследствие снижения тонуса НПЗВД и пищеводно-желудочного градиента давления, особенно выраженное у пациентов со стенозом 12-перстной кишки. После резекции желудка, особенно в первый год после операции, наступало прогрессирование признаков НЗФК и увеличение числа пациентов с рефлюкс-эзофагитом, что указывает, по ее мнению, на необходимость одновременно с основным оперативным вмешательством по поводу язвенной болезни (резекцией желудка) выполнять антирефлюксные операции. А.И.Горбашко и соавт. [4], Ю.Е.Березов и соавт. [83] также считали, что профилактическое применение антирефлюксных операций при резекции желудка у пациентов с НЗФК должно быть обязательным элементом. В.М.Буянов и соавт. [14], А.И.Горбашко и соавт. [84] проводили обязательную коррекцию кардии при ее недостаточности, когда в объем оперативного вмешательства был включен любой вид ваготомии. Другую точку зрения имеют А.Ф.Черноусое и соавт. [40] считая, что коррекцию НЗФК, сочетанной с язвой 12-перстной кишки или желудка, нужно проводить только при выраженном рефлюкс-ззофагите и полагали, что резекция желудка по Бильрот — 2 устраняет пептический фактор и тем нивелирует развитие рефлюкс-эзофагита.
При сочетании ГЭРБ с желчнокаменной болезнью показания к коррекции кардии В.А.Кубышкин и соавт. [85] делят на абсолютные и относительные. К абсолютным показаниям они относили: наличие грыжи пищеводного отверстия диафрагмы, которой свойственны все осложнения рефлюкса; пульмональная или ларингеальная симптоматика желудочно-пищеводного рефлюкса, пищевод Баррета. Относительными показаниями к симультанным антирефлюксным операциям они считали: большую длительность заболевания и отсутствие эффекта от комплексной антирефлюксной терапии, наличие рентгенологически документированного рефлюкса, эндоскопические признаки эзофагита 2-3 ст. по Savary-Miller, подтвержденные данными биопсии, давление в НПЗВД ниже 15-10 мм.рт.ст., рН ниже 4,0 на протяжении 10% всего времени исследования, нарушение моторики пищевода. К.В.Пучков и соавт. [86, 87], А.Г.Хитарьян и соавт. [17] сообщили о возможности одномоментного хирургического лечения триады Кастена (хронической язвы 12-перстной кишки, желчнокаменной болезни и грыжи пищеводного отверстия диафрагмы) видеолапароскопическим способом.
Нами было проведено оперативное лечение 397 больным гастроэ-зофагеальной рефлюксной болезнью, сочетанной с различными заболеваниями органов брюшной полости. Выделяли абсолютные, настойчивые и относительные показания к операции (табл. 5.9).
Из таблицы видно, что большинство больных (323 чел., 81,4%) оперировали по абсолютным и настойчивым показаниям. По абсолютным показаниям оперированы больные из-за метаплазии эпителия слизистой оболочки пищевода по желудочному или кишечному типу с высоким риском малигнизации дистального его отдела (пищевод Баррета) или не возможности адекватного питания вследствие стенозирующего рефлюкс-эзофагита. Коррекцию замыкательной функции кардии, независимо от того имеется или не имеется ее недостаточность, выполняли всегда, когда производили селективную проксимальную ваготомию, т.к. эта операция приводит к разрушению анатомических образований этой зоны.
Таблица 5.9
Показания к хирургическому лечению гэрб
Показания к хирургическому лечению | Число больных | ||
n | % р±m | ||
Абсолютные | стенознрующий рефлюкс-эзофагит | 5 | 1.3=0,5 |
РЭ с метаплазией слизистой оболочки пищевода (пищевод Баррета) | 3 | 0,8±0,4 | |
при СПВ у больных ХДЯ независимо от наличия ГЭРБ | 115 | 28,9+2,3 | |
Настойчивые | ГПОД с наличием катарального, эрозивного язвенного или хронического РЭ | 122 | 30,7+2,3 |
РЭ с укорочением пищевода (приобретенньгё короткий пищевод) | 11 | 2,8±0,8 | |
эрозивно-язвенный РЭ, осложненный кровотечением с явлениями хронической анемии | 6 | 1,5+0,6 | |
гастроэзофагеальный рефлюкс с признаками рефлекторной стенокардии | 2 | 0,5+0,3 | |
гастроэзофагеальный рефлюкс с наличием псевдокоронарных болей | 3 | 0,8±0,4 | |
гастроэзофагеальньгй рефлюкс с ларингеальной или пульмональной симптоматикой | 10 | 2,5±0,7 | |
при резекции желудка у больных ХГДЯ с )аличием РЭ | 34 | 8,6±1,4 | |
триада Кастена | 7 | 1,7±0,6 | |
при ЛХЭ при наличии у больных ГЭРБ с явлениями РЭ, не поддающегося консервативному лечению | 5 | 1,3+0,5 | |
Относительные | при резекции желудка или холецистэктомии, выполняемых соответственно по поводу ХГДЯ и ЖКБ, наличие у этих больных ГЭРБ с закислением пищевода более 12 мин/час, снижением коэффициента (отношение давления в НПЗВД к внутрижелудочному) менее 2,5:1, укорочением НПЗВД менее 3 см | 74 | 8,6±1,9 |
Всего | 397 | 100 | |
Настойчивыми показаниями к операции считали бесперспективность медикаментозных методов лечения при наличии грубых морфологических изменений в пищеводе или выраженных экстрапищеводных проявлений ГЭРБ, снижающих качество жизни больного. У каждого третьего из этих больных имелось сочетание гастроэзофагеальной рефлюксной болезни с грыжей ПОД, при которой наличие клинических проявлений НЗФК консервативная терапия имеет только симптоматическое значение и непродолжительный эффект в момент ее проведения.
По относительным показаниям оперативное лечение выполнено у 74 больных (18,6%) с признаками ГЭРБ, выявляющимися инструментальными методами. Характеристики патологического ЖПР у этих больных, по нашим наблюдениям, без коррекции в последующем приводят к развитию пищеводных и внепищеводных осложнений.
Целью оперативных вмешательств, направленных на устранение патологического желудочно-пищеводного рефлюкса являлась ликвидация причин, приведших к возникновению ГЭРБ и восстановление замыкательной функции физиологической кардии с учетом выявленных в ней нарушений.
Диагностика и хирургическое лечение гастроэзофагеальной рефлюксной болезни
Диагностика и хирургическое лечение гастроэзофагеальной рефлюксной болезни
В.И. Оскретков, В.А. Ганков, А.Г. Климов, А.А. Гурьянов
Кафедра общей хирургии Алтайского государственного медицинского университета; МУЗ “Городская больница N 12”, г. Барнаул, Россия
В работе рассматриваются актуальные вопросы диагностики и лечения гастроэзофагеальной рефлюксной болезни. Анализируются данные о 426 больных. Проведена оценка результативности диагностики недостаточности замыкательной функции кардии (НЗФК). Рентгенологические методы позволили диагностировать НЗФК у 81,5% больных, эзофагоскопия — у 73,9%. Эзофагоскопия позволила установить, что среди больных гастроэзофагеальной рефлюксной болезнью, осложненной рефлюкс-эзофагитом, 80,7% имели грыжу пищеводного отверстия диафрагмы. При эзофагоскопии выявляется пролапс слизистой оболочки желудка в пищевод у 11,8% больных. Диагностическую значимость имеют pH-метрия, проба Бернштейн-Беккера, манометрия пищеводно-желудочного перехода.
Для хирургического лечения гастроэзофагеальной рефлюксной болезни рекомендуется видеолапароскопическая эзофагофундопликация.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, диагностика, лечение
Несмотря на повышенный интерес исследователей к этиологии и патогенезу гастроэзофагеальной рефлюксной болезни (ГЭРБ), до настоящего времени у специалистов нет единых представлений о запирательных механизмах кардии [4; 10; 12], не выяснены причины развития ГЭРБ у больных различными хроническими заболеваниями органов брюшной полости. И все же при достигнутых успехах медикаментозной терапии ГЭРБ и ее осложнений довольно часто курс лечения желаемого результата не дает. Или зачастую, несмотря на видимое излечение, через короткий промежуток времени наступает рецидив симптомов, а желудочно-пищеводный рефлюкс осложняется метаплазией эпителия, стенозом или рубцовой деформацией и укорочением пищевода [2; 3]. Многие предложенные методы хирургической коррекции ГЭРБ (более 40) недостаточно эффективны. В последние годы оправдано стремление хирургов к применению в лечении этого заболевания малоинвазивных видеоэндоскопических операций, отличающихся меньшей травматичностью [6; 9; 12]. Но как в “открытой” хирургии, так и в “закрытой” разнообразен диапазон методик коррекции ГЭРБ [3; 9; 11]. Подвергаются обсуждению показания, техника и детали операции [1; 7; 8; 9; 13]. Требуется накопление опыта для оценки результатов “закрытых” вмешательств, число которых в нашей стране невелико.
Материалы и методы
Проанализированы результаты обследования и лечения 426 больных с гастроэзофагеальной рефлюксной болезнью, сочетанной с различными заболеваниями органов пищеварения.
Среди наблюдавшихся 426 больных мужчин было 55,2%, женщин — 44,8%. Большинство пациентов (364 чел., 86,3%) находились в наиболее работоспособном возрасте. В зависимости от заболеваний, способствующих возникновению ГЭРБ, все больные были условно разделены на четыре группы. Первую группу составили пациенты с аксиальными грыжами пищеводного отверстия диафрагмы (ГПОД) — 114 чел. (26,8%), вторую группу — с хронической гастродуоденальной язвой (ХГДЯ) — 157 чел. (36,8%), третью — с желчно-каменной болезнью (ЖКБ) — 78 чел. (18,3%), четвертая группа объединяла больных с различными сочетаниями заболеваний: ГПОД, ХГДЯ и ЖКБ — 77 чел. (18,1%).
Для диагностики ГЭРБ, ее осложнений и контроля за эффективностью лечения наряду с общепринятыми методиками клинического, лабораторного и инструментального исследования (рентгеноскопия, эндоскопия, УЗИ) применялись специальные методы: внутрипищеводная рН-метрия, проба Бернштейн-Беккера, тест клиренса пищевода, манометрия пищеводно-желудочного перехода. Помимо этого, изучалось влияние величины угла Гиса и расстояния между ножками диафрагмы на замыкательную функцию кардии, а также показателей кислотовыделительной функции желудка на частоту и выраженность рефлюкс-эзофагита.
Результаты исследования
Клиническая симптоматика ГЭРБ обусловлена патологическим желудочно-пищеводным рефлюксом и его осложнениями. Частью смешанных симптомокомплексов были проявления сопутствующих заболеваний. Основной жалобой являлась боль — у 379 чел. (88,9%), которая наиболее часто локализовалась в эпигастральной области и под мечевидным отростком. Загрудинные боли у большинства встречались при наличии у них тяжелых форм рефлюкс-эзофагита (РЭ) — у 59 из 73 чел. Наиболее специфичным симптомом ГЭРБ была изжога, выявленная у 219 чел. (51,4%), чаще появляющаяся после переедания, приема большого количества сладостей, пряностей или острых блюд, реже — натощак. Отрыжка и срыгивание выявлены у 228 чел. (53,5%), из них отрыжка только воздухом — у 155 чел. (36,4%), воздухом и пищей — у 73 пациентов (17,1%). У двух больных наблюдали аэрофагию. Немало пациентов (44 чел., 10,3%) страдали “симптомом шнурков”, проявляющимся вытеканием пищи из желудка в рот при наклонах туловища вперед. Ночная регургитация пищи из желудка в рот — “симптом мокрой подушки” — выявлена только у семи чел. (1,6%). Жалобы на дисфагию предъявил 21 чел.(4,9%). Головокружение при анемии, обусловленной диапедезным кровотечением из эрозивной поверхности пищевода, было у шести больных (1,4%), но лишь у одного из них была резко выраженная анемия. Ларингеальная и пульмональная симптоматика выявлена у 10 больных (2,4%), страдающих “симптомами шнурков” и (или) “мокрой подушки”. Проявления этого — периодическая осиплость голоса после ожога глотки и гортани кислым желудочным содержимым, частые обострения хронического бронхита и пневмонии, обусловленные частичной регургитацией содержимого желудка в дыхательные пути. Пять человек отмечали боли в области сердца.
Анализ клинических проявлений ГЭРБ показал, что наиболее выраженная клиника заболевания встречалась у больных ГПОД и при ее сочетании с другой патологией органов пищеварения, а также у больных гастростазом, развившимся по тем или иным причинам.
Рентгенологический метод позволил диагностировать недостаточность замыкательной функции кардии (НЗФК) у 81,5±1,9% больных, имевших ее клинические проявления. Это обследование дало возможность документировать обнаруженную патологию, выявить причину, способствующую развитию ГЭРБ (ГПОД, пилородуоденальный язвенный стеноз и пр.). Рентгенологическое определение желудочно-пищеводного рефлюкса (ЖПР) в вертикальном положении указывало на более выраженную недостаточность замыкательной функции кардии (НЗФК). Считали, что притупление угла Гиса, по рентгенологическим данным, может служить косвенным диагностическим признаком НЗФК и ГПОД. Рентгенологическое исследование позволило выявить наличие рефлюкс-эзофагита лишь у 103 больных, что более чем в два раза меньше, чем при эзофагоскопии (231 чел.). В основном не определялись поверхностные формы пептических поражений слизистой оболочки пищевода: у 46 больных — хронический рефлюкс-эзофагит, у 59 чел. — катаральный рефлюкс-эзофагит. Наряду с этим рентгенологический метод позволил выявить у 11 чел. (9,6%) короткий приобретенный пищевод I-II степени (рис. 1), уточнить протяженность и диаметр пептической стриктуры у девяти больных со стенозирующим рефлюкс-эзофагитом, установить степень ГПОД у других больных, что существенно дополняло информацию при обследовании другими методами.
При эзофагоскопии НЗФК обнаружена у 73,9±2,1% больных. Метод оказался высокоинформативен в диагностике рефлюкс-эзофагита. В своей работе мы использовали усовершенствованную нами классификацию пептического эзофагита В.М. Араблинского (1965), в которой в зависимости от выраженности макроскопических изменений различали четыре степени последовательного развития рефлюкс-эзофагита — катаральный, эрозивный, язвенный и стенозирующий (прогрессирующий фиброз с рубцовым сужением пищевода). Помимо этого, выделяли хроническую форму эзофагита, поскольку часть больных была госпитализирована в фазу ремиссии между частыми обострениями заболевания. У 123 больных был выявлен катаральный рефлюкс-эзофагит, у 36 — эрозивный, у 12 — язвенный и у 11 пациентов — стенозирующий рефлюкс-эзофагит. 49 больных имели хронический рефлюкс-эзофагит. У 189 человек (45,0%) ГЭРБ протекала без морфологических изменений в слизистой оболочке пищевода. Соотношение тяжести рефлюкс-эзофагита в различных группах больных показало, что наиболее часто ГЭРБ осложнялась рефлюкс-эзофагитом у лиц, имевших ГПОД (80,7%) при различных сочетанных заболеваниях (61,0%). ХГДЯ в качестве осложнения встречалась примерно у половины больных (47,1%) и реже всего — у больных ЖКБ (25,0%). Тяжесть течения рефлюкс-эзофагита не имела прямой зависимости от давности заболевания.
При эзофагоскопии выявлено, что пролапс слизистой оболочки желудка в пищевод определяется при отсутствии ГПОД у 11,8±2,1% больных. Возможно, это происходило вследствие более выраженного и подвижного подслизистого слоя в пищеводно-желудочном переходе в момент транзиторного расслабления кардии, инсуффляции воздуха и введения эндоскопа. Исходя из этого указанный эндоскопический признак считаем необязательным и непатогномоничным для ГПОД. Помимо этого, сомкнутость или зияние кардии в момент эндоскопического исследования не может свидетельствовать о выраженности НЗФК.
Гистологическое исследование во время эзофагоскопии выполнили 23 больным с подозрением на метаплазию эпителия пищевода и злокачественный процесс в стенке пищевода. Во всех исследуемых материалах отмечалось отсутствие атипичных клеток, в тканях определялось хроническое воспаление, иногда встречались участки грануляционной ткани, фибринозного некроза, инфильтрированные лейкоцитами. В одном препарате в покровном эпителии были явления паракератоза и незначительного акантоза. В трех наблюдениях имелась метаплазия эпителия пищевода по желудочному и кишечному типу, классифицированная нами как пищевод Баррета.
Патологический желудочно-пищеводный рефлюкс вследствие наличия ГЭРБ выявлен рН-метрией у 91,5±1,5% больных, что свидетельствует о его высокой диагностической ценности в выявлении этой патологии.
Пробу Бернштейн-Беккера проводили для подтверждения рефлюкс-эзофагита и вызванной им симптоматики. Для этого больному через рот до нижней трети пищевода вводили тонкий зонд, через который с помощью шприца поочередно орошали слизистую оболочку пищевода 0,1%-ным раствором хлористоводородной кислоты и физиологическим раствором в течение одной минуты. Проба считалась положительной у больного с рефлюкс-эзофагитом, когда введение кислоты сопровождалось жжением по ходу пищевода, болью за грудиной, чувством изжоги. При отсутствии указанных жалоб пробу считали отрицательной. В момент выяснения информативности пробы Бернштейн-Беккера у 346 чел. оказалось, что она была отрицательной почти у двух третей больных, имевших пептический эзофагит. Между тем как у одной трети лиц контрольной группы и у 37,8% больных ГЭРБ без морфологических изменений в пищеводе возникло жжение за грудиной, характеризующее пробу положительной. Вследствие этого мы пришли к выводу, что в диагностике рефлюкс-эзофагита проба Бернштейн-Беккера малоинформативна.
Клиренсом пищевода называют время восстановления внутрипищеводного рН после искусственного или естественного его закисления. Показатели теста клиренса пищевода у 346 больных, включая 42 чел. контрольной группы, характеризующие скорость очищения его просвета от введенной кислоты, показали, что примерно у одной трети больных рН-пищевода после проведенного теста не приходил в норму в течение 30 минут и более. При этом у большинства больных не было пептического эзофагита, а при наличии его поверхностных форм клиренс пищевода даже улучшался. В итоге разноречивая информация заставила нас признать этот тест неинформативным, а технологию его проведения — не соответствующей реальному воспроизведению самоочищения пищевода.
Манометрия пищеводно-желудочного перехода позволила оценить состояние физиологической кардии у 447 человек, включая 36 чел. контрольной группы. Выявлены основные механизмы и характерные особенности развития ГЭРБ у больных различными заболеваниями органов пищеварения (табл. 1). Так, у большинства больных ГПОД основной причиной НЗФК было укорочение протяженности нижней пищеводной зоны высокого давления (НПЗВД) до 1,84±0,04 см и повышение внутриполостного давления в желудке до 9,53±0,91 мм рт. ст. У больных ХГДЯ ГЭРБ развивалась на фоне низкого давления в НПЗВД (14,24±0,27мм рт. ст.).
Расстояние между ножками диафрагмы нами измерено интраоперационно у 397 человек с ГЭРБ. Более чем у половины больных — у 253 чел. (63,7±2,4%) — расстояние между ножками диафрагмы было не изменено и соответствовало 3,5-4 см. Если имелось расширение пищеводного отверстия диафрагмы, то оно обычно не превышало 4-7 см. Более 7 см — расстояние между диафрагмальными ножками лишь у семи больных. Расширение пищеводного отверстия диафрагмы было более характерным для больных ГПОД в сочетании ее с другими заболеваниями, что может служить интраоперационным диагностическим признаком этого заболевания. Зависимости тяжести рефлюкс-эзофагита и величины расстояния между ножками диафрагмы не прослеживалось.
Анализ результатов исследования кислотовыделительной функции желудка у 252 больных ГЭРБ коррелятивной зависимости тяжести рефлюкс-эзофагита от показателей объема секреции и кислотности желудочного сока не выявил. Следовательно, показатели кислотности желудочного сока у больных ГЭРБ решающего значения в развитии рефлюкс-эзофагита не имеют. Существеннее наличие ЖПР, его интенсивность, высота и продолжительность задержки рефлюктанта в пищеводе.
В основе ГЭРБ у больных ЖКБ было повышенное внутрижелудочное давление (8,15±0,45 мм рт. ст.), способствовавшее уменьшению пищеводно-желудочного градиента давления, что при небольшом снижении давления в кардии и малом его укорочении приводило к срыву механизмов компенсации ее замыкательной функции.
Анализ полученных данных во всех группах больных выявил обратную корреляционную зависимость тяжести рефлюкс-эзофагита от длины кардии (r = — 0,387) и состояния тонуса НПЗВД (r = — 0,436). С укорочением длины кардии наблюдались более выраженные морфологические изменения в слизистой оболочке пищевода. Так, длина кардии при стенозирующем рефлюкс-эзофагите была почти в три раза меньше длины кардии у больных, не имевших пептического эзофагита. Снижение тонуса НПЗВД также способствовало развитию более тяжелых морфологических изменений в стенке пищевода, у лиц со стенозирующим рефлюкс-эзофагитом тонус НПЗВД был более чем в два раза ниже по сравнению с больными, не имевшими их. Показатели пищеводно-желудочного градиента давления (ПЖГД) и коэффициента (отношение тонуса НПЗВД к внутрижелудочному давлению) не отличались от величин группы контроля у больных хроническим рефлюкс-эзофагитом и у пациентов, не имевших морфологических изменений в пищеводе. Однако у лиц с более тяжелыми проявлениями ГЭРБ они были в два и более раза ниже величин физиологической нормы.
Нарушение перистальтики пищевода регистрировали у 10,5% больных ГЭРБ. У 37 больных отмечалось снижение амплитуды перистальтических сокращений до 28,4±1,2 мм рт. ст., учащение ритма сокращений (повышение скорости распространения волны), увеличение скорости подъема волны и ее падения (укорочение продолжительности сокращения). Мы характеризовали это состояние перистальтики как “раздраженный пищевод”. Изменения в основном были характерны для пациентов с острыми формами пептического эзофагита — от катаральных до язвенных морфологических изменений. Обычно после успешного консервативного лечения рефлюкс-эзофагита или после операции нормальная пищеводная перистальтика восстанавливалась. У шести больных со стенозирующим рефлюкс-эзофагитом наблюдали редкие сокращения пищевода (до 2,7±0,8 в 1 мин.) малой силы и третичные перистальтические волны, которые, как известно, не имеют пропульсивной силы. Исследование пропульсивной функции пищевода важно при необходимости хирургического вмешательства и предотвращении послеоперационной дисфагии для больных пептическим эзофагитом.
По абсолютным показаниям оперированы пациенты, у которых наблюдалась метаплазия эпителия слизистой оболочки пищевода по желудочному или кишечному типу с высоким риском малигнизации дистального его отдела (пищевод Баррета) или невозможности адекватного питания вследствие стенозирующего рефлюкс-эзофагита. Коррекцию замыкательной функции кардии независимо от того, имеется или не имеется ее недостаточность, выполняли всегда, когда производили селективную проксимальную ваготомию, т. к. эта операция приводит к разрушению анатомических образований этой зоны.
Настойчивыми показаниями к операции считали бесперспективность медикаментозных методов лечения при наличии грубых морфологических изменений в пищеводе или выраженных экстрапищеводных проявлений ГЭРБ, снижающих качество жизни больного. У каждого третьего из этих больных имелось сочетание гастроэзофагеальной рефлюксной болезни с грыжей ПОД, при которой наличие клинических проявлений НЗФК консервативная терапия имеет только симптоматическое значение и непродолжительный эффект в момент ее проведения.
По относительным показаниям оперативное лечение выполнено 74 больным (18,6%) с признаками ГЭРБ, выявляющимися инструментальными методами. Характеристики патологического ЖПР у этих больных, по нашим наблюдениям, без коррекции в последующем приводят к развитию пищеводных и внепищеводных осложнений. Целью оперативных вмешательств, направленных на устранение патологического желудочно-пищеводного рефлюкса, являлась ликвидация причин, приведших к возникновению ГЭРБ, и восстановление замыкательной функции физиологической кар-дии с учетом выявленных в ней нарушений.
Показания к экстирпации пищевода с эзофагопластикой возникли лишь у двоих больных ГПОД, страдающих ГЭРБ, осложненной стенозирующим рефлюкс-эзофагитом.
Для хирургического лечения ГЭРБ применяется разработанная нами дозированная видеолапароскопическая эзофагофундопликация, предусматривающая индивидуализацию характера вмешательства с учетом патогенетических факторов, вызвавших ГЭРБ (свидетельство на изобретение № 1835265 от 13.10.92 г.). Детально отработаны техника операции (рис. 3), расположение операционной бригады, выбраны оптимальный набор инструментального оснащения, методика интраоперационной манометрии. Использовали пять лапаропорт, два видеомонитора. Положение больного на спине с приподнятым головным концом операционного стола и небольшим поворотом направо. Электрокрючком прецизионно, пристеночно, малыми порциями снимали верхний листок брюшины малого сальника на 3-4 см ниже пищеводно-желудочного перехода с послойным скелетированием кардии, дна желудка и 4-5 см абдоминального отдела пищевода, не углубляясь в толщу тканей, каждый раз возвращаясь от начала мобилизации органов. После того как вскрывалось окно в малом сальнике, под контролем зрения мобилизовывали заднюю стенку пищевода до ножек диафрагмы и входа в заднее средостение, дно желудка до первых коротких желудочных сосудов. Перед формированием фундопликационной манжетки производили позиционирование зонда калибровочного устройства.
Формирование манжетки начинали со скелетированного участка желудка путем перитонизации малой кривизны ручным либо аппаратным (Endostitch) непрерывным швом, постепенно увеличивая конус манжетки из передней и задней стенок желудка, переходили на пищевод (3-4 см) с захватом в шов его правого “ребра” под контролем интраоперационного давления в кардии с помощью датчиков давления на приборе. Непрерывный шов на манжетке заканчивали интракорпоральным узлом (рис. 6). Индивидуализация характера вмешательства осуществлялась с учетом коэффициента, характеризующего отношение давления в НПЗВД к давлению в желудке. Коэффициент учитывался при выборе оптимальной степени сдавления пищевода и длины манжетки на калибровочном устройстве.
Большинство интраоперационных осложнений при видеолапароскопической фундопликации было специфичным и произошло при первых 16 операциях. Мы считаем, что они обусловлены нашими недостаточными навыками в эндоскопической хирургии кардиоэзофагеальной зоны. Все эти осложнения были клинически малозначимы и не привели к увеличению сроков послеоперационного периода. Наиболее существенные среди них — у двоих больных во время операции после мобилизации пищевода наступило микроповреждение левой плевральной полости с развитием напряженного пневмоторакса, который купировали плевральным дренажом и снижением давления в брюшной полости до 8-10 мм рт. ст.
Длительность закрытых операций — от 60 до 120 минут и в среднем составила 85,5±5,5 мин.
После видеолапароскопической дозированной эзофагофундопликации у двух пациенток (1,4%) произошел рецидив заболевания, хотя у одной из них возник частичный возврат симптомов патологического желудочно-пищеводного рефлюкса.
В отдаленные сроки до пяти лет отличный и хороший результат после видеолапароскопической фундопликации получили 96,5±1,5% больных, удовлетворительный — у 2,1±1,1% и плохой — 1,4±0,9% пациентов. Результаты манометрии пищеводно-желудочного перехода после видеолапароскопической фундопликации почти не отличались от физиологической нормы.
Таким образом, видеолапароскопическая дозированная эзофагофундопликация у больных гастроэзофагеальной рефлюксной болезнью в сочетании с хроническими заболеваниями органов пищеварения является наиболее оптимальным методом коррекции замыкательной функции кардии. Воздействие на основные факторы, вызвавшие ее недостаточность (протяженность и тонус нижней пищеводной зоны высокого давления, пищеводно-желудочный градиент давления), и их выраженность следует учитывать индивидуально у каждого из пациентов.
Список литературы
1. Балалыкин, А.С. Эндоскопическая абдоминальная хирургия./ А.С. Балалыкин, О.Э. Луцевич, В.П. Сажин, А.В. Оноприев, А.В. Федоров. — Москва, 1996. — 150 с.
2. Вуколов, А.В. Рефлюкс-эзофагит: терапия или хирургия / А.В. Вуколов, В.А. Кубышкин // Эндоскоп. хирургия. — 1996. — № 1. — С. 25-29.
3. Кубышкин, В.А. Гастроэзофагеальная рефлюксная болезнь./ В.А. Кубышкин, Б.С. Корняк. — М. — 1999. — 189 с.
4. Лапкин, К.В. Эндохирургическое лечение гастроэзофагеального рефлюкса / К.В. Лапкин, А.Е. Климов // Эндоскоп. хирургия. — 1996. — № 4.
5. Луцевич, О.Э. Новые возможности хирургического лечения рефлюксных заболеваний пищевода / О.Э. Луцевич, С.А. Гордеев, Ю.А. Прохоров // Эндоскоп. хирургия. — 1996. -№ 4. — С. 24.
6. Никитенко, А.И. Лапароскопические антирефлюксные операции на пищеводе / А.И. Никитенко, Е.Г. Никитенко, А.М. Желаннов // Эндоскоп. хирургия. — 1998. — № 1. — С. 32.
7. Оноприев, В.И. Этюды функциональной хирургии язвенной болезни. — Краснодар, 1995. — С. 293.
8. Оскретков, В.И. Видеолапароскопическая дозированная эзофагофундопликация у больных с гастроэзофагеальной рефлюксной болезнью / В.И. Оскретков, В.А. Ганков, А.Г. Климов // Эндоскоп. хирургия. — 2002. — № 3. — С. 39.
9. Пучков, К.В. Профилактика ранней дисфагии в антирефлюксной хирургии / К.В. Пучков, В.Б. Филимонов, О.Э. Карпов и др. // Эндоскоп. хирургия. — 2001. — № 3. — С. 69.
10. Ривкин, В.Л. Лапароскопическая фундопликация: Обзор тезисов 5-го Международного конгресса по эндоскопической хирургии // Эндоскоп. хирургия. — 1997. — № 1. — С. 34-36.
11. Сигал, Е.И. Малоинвазивная хирургия в лечении диафрагмальных грыж / Е.И. Сигал, М.В. Бурмистров // Всероссийская научная конференция “Актуальные проблемы хирургии”, посвященная 130-летию со дня рождения проф. Н.И. Напалкова: Сб. науч. тр. — Ростов-на-Д, 1998. — С. 61-62.
12. Хитарьян, А.Г. Лапароскопическая коррекция недостаточности кардии у больных с заболеваниями органов брюшной полости / А.Г. Хитарьян, И.А. Абоян // Второй конгресс Ассоциации хирургов: Материалы. — СПб., 1998. — С. 337.
13. Montori, A. Gastroesophageal Reflux Disease. Laparoscopic Anti-reflux Procedures. / A. Montori, L. Mansoni, M. Gasparrini, J. Montori //Gastroent. Int. 1997; 10: 38-42.
14. Nissen, R. Gastropexy and “Fundoplication” in Surgical Managment of Hiatal Hernia./ R. Nissen.// Am. J. Dig. Dis. 1961; 6: 954.
Статья опубликована на сайте http://www.gastroscan.ru
Рефлюкс-эзофагит (ГЭРБ) — цены лечение, симптомы и диагностика рефлюкс-эзофагита (ГЭРБ) в «СМ-Клиника»
Нужна дополнительная информация?
Спасибо за обращение.
Ваша заявка принята. Наш специалист свяжется с Вами в ближайшее время
Нужна дополнительная информация?
Не нашли ответ на свой вопрос?
Оставьте заявку и наши специалистыпроконсультируют Вас.
Спасибо за обращение.
Ваша заявка принята. Наш специалист свяжется с Вами в ближайшее время
Спасибо за обращение.
Ваша заявка принята.
Наш специалист свяжется с Вами в ближайшее время
Симптомы гастроэзофагеальной рефлюксной болезни
Характерные симптомы гастроэзофагеальной рефлюксной болезни — изжога, боли в области грудины, кислая отрыжка, срыгивание, тошнота, болезненное и затрудненное прохождение пищи, дискомфорт после приема пищи, метеоризм. Погрешности в диете (употребление жирного, газированных напитков, алкоголя), курение, физические нагрузки, ношение одежды с тугим поясом могут провоцировать усиление симптомов.Гастроэзофагеальная рефлюксная болезнь (ГЭРБ, рефлюкс-эзофагит) – одно из самых распространенных заболеваний пищевода, эпизодически его симптомы, в первую очередь изжога, возникают у половины взрослого населения страны, мужчины и женщины болеют одинаково часто, как правило в возрасте от 20 до 45 лет.
ГЭРБ — болезнь коварная, без должного лечения она может привести к серьезным осложнениям, в том числе к раку пищевода. Опасность усугубляется тем, что несмотря на массу малоприятных симптомов, портящих им жизнь, многие люди не спешат обращаются к врачу, предпочитая приглушать симптомы таблетками от изжоги.
Причины возникновения и течение ГЭРБ
Факторами способствующими развитию ГЭРБ считаются грыжа пищеводного отверстия диафрагмы (грыжа пищевода) стресс, ожирение, беременность, курение, прием некоторых лекарств (антагонисты кальция, антихолинергические препараты, бетаблокаторы и др.).
Непосредственной причиной гастроэзофагеальной рефлюксной болезни является длительный контакт желудочного содержимого со слизистой оболочкой пищевода. Нарушение моторики приводит к тому что кислая желудочная среда не только попадает в пищевод, но и находится там длительное время.
Неправильная работа (слабость) нижнего пищеводного сфинктера, который должен препятствовать обратному движению масс, обуславливает попадание желудочного содержимого в пищевод, а недостаточная перистальтика пищевода и снижение пищеводного клиренса являются причиной медленного опорожнения желудка и вывода этой агрессивной среды. Подобный дисбаланс защитных функций и приводит к развитию рефлюкс-эзофагита.
Длительное воздействие кислоты и желчи на слизистую пищевода приводит к ее хроническому воспалению и эрозивно-язвенным изменениям, очаги измененной слизистой нижних отделов пищевода часто служат источником роста раковой опухоли.
На начальных стадиях заболевания отмечают отдельные области эрозии дистального отдела пищевода, на второй стадии отдельные очаги воспаления сливаются в общую область, далее на третьей стадии воспалительный процесс охватывает всю поверхность слизистой, появляются язвы. Четвертая стадия — это хроническая язва пищевода, стеноз, цилиндрическая метаплазия слизистой пищевода (пищевод Барретта).
Больные рефлюксной болезнью подвержены повышенному риску приобретения различных заболеваний придаточных пазух носа, заболеваний трахеи, гортани и легких (ишемическая болезнь сердца со стенокардией и/или c нарушениями сердечного ритма, рефлюксные ларингит и фарингит, рецидивирующие пневмонии, бронхиальная астма, эрозии зубов и др).
Вот к каким результатам может привести «обычная изжога»!
Если у Вас наблюдаются подобные симптомы, советуем записаться на прием к врачу. Своевременная консультация предупредит негативные последствия для вашего здоровья. Телефон для записи +7 (495) 292-39-72
Диагностика гастроэзофагеальной рефлюксной болезни (ГЭРБ)
Для диагностики ГЭРБ используется различные методы. Основным методом является эндоскопический — он позволяет получить подтверждение наличия рефлюкс-эзофагита, оценить степень его тяжести. Гистологический анализ биоптатов слизистой оболочки пищевода дает дополнительную информацию с степени дистрофических изменений эпителиального слоя.Контрастная рентгенография пищевода позволяет выявить рефлюкс как таковой, т. е. зафиксировать попадание контраста из желудка в пищевод. Рентгенологическое исследование пищевода также может указать наличие грыжи пищеводного отверстия диафрагмы, стриктуры пищевода, диффузного эзофагоспазма диафрагмы.
Манометрия пищевода (эзофагоманометрия) — позволяет оценить сократительную активность пищевода, изучить показатели движения его стенки и деятельности пищеводных сфинктеров.
Лечение гастроэзофагеальной рефлюксной болезни (ГЭРБ)
После проведения комплексной диагностики, врач-гастроэнтеролог всесторонне оценивает состояние здоровья пациента, анализирует степень тяжести и характер протекания заболевания и подбирает индивидуальную схему лечения.Цель лечения гастроэзофагеальной рефлюксной болезни заключается в купировании ее симптомов, лечении эзофагита, предотвращении или устранении осложнений заболевания, улучшении качества жизни больного. Лечение ГЭРБ может быть консервативным и хирургическим.
Консервативное лечение гастроэзофагеальной рефлюксной болезни (ГЭРБ)
Консервативное лечение показано при легкой и средней степени рефлюксной болезни.Правильно подобранная антирефлюксная терапия позволяет уменьшить рефлюкс, снизить повреждающие свойства рефлюктата (желудочного содержимого), улучшить пищеводный клиренс и защиту слизистой оболочки пищевода.
В основе эффективного антирефлюксного лечения лежит изменение образа жизни, в частности необходимо нормализовать массу тела, серьезно скорректировать диету, объем и время приема пищи (избегать употребления жирного, кислого, продуктов, усиливающих газообразование, а также шоколада, кофе, газированных напитков). Очень важно исключить курение и употребление алкоголя, следует воздержаться от приема препаратов угнетающих функцию нижнего пищеводного сфинктера. Пациенты должны избегать переедания, а так же нагрузки на мышцы брюшного пресса.
Антирефлюксная медикаментозная терапия включает в себя регулярный прием антацидов и производных альгиновой кислоты, прокинетиков и антисекреторных препаратов, которые снижают кислотность желудочного сока, защищают слизистую оболочку пищевода, активизируют перистальтику, усиливают активность пищеводных сфинктеров и улучшают моторику пищевода и желудка в целом.
При комплексной медикаментозной терапии рефлюкс-эзофагита средней тяжести у большинства пациентов наблюдается значительное уменьшение симптомов и улучшение качества жизни.
Базовый курс лечения должен составлять не менее одного месяца, а затем в течение 6-12 месяцев больной должен получать поддерживающее лечение. Без поддерживающего лечения велика вероятность рецидива эрозивного эзофагита — она доходит до 90% в течение года.
Следует иметь в виду, что многие антацидные препараты содержат в своем составе большое количество алюминия, и соответственно длительный, бессистемный их прием приводит к накоплению его в организме, что в старости увеличивает риск развития болезни Альцгеймера.
Хирургическое лечение гастроэзофагеальной рефлюксной болезни (ГЭРБ)
Вопрос об оперативном лечении ГЭРБ возникает, когда консервативная терапия не дает ожидаемого эффекта, несмотря на неоднократные курсы медикаментозной терапии и соблюдение всех рекомендаций по нормализации образа жизни. Консервативное лечение позволяет снизить остроту симптомов и не дать развиться осложнениям, но не устраняет причину заболевания.Если, несмотря на активное медикаментозное лечение ГЭРБ, вас больше года продолжают мучить изжога, боли и другие симптомы рефлюксной болезни, то самое время задуматься о консультации с опытным хирургом.
Показанием к хирургическому лечению рефлюкс-эзофагита также является осложненное течение заболевания: кровотечения, язвенные поражения, пептические стриктуры пищевода, развитие пищевода Барретта с дисплазией эпителия высокой степени. Особенно часто показания к операции возникают при сочетании ГЭРБ с грыжей пищеводного отверстия диафрагмы.
В «СМ-Клиника» работают опытные хирурги которые успешно проводят хирургическое лечение гастроэзофагеальной рефлюксной болезни.
Узнать подробности и записаться на прием к специалисту вы можете по телефону +7 (495) 292-39-72
Наши преимущества:

Более 120 ведущих гастроэнтерологов и хирургов

Все специалисты
в одной клинике

Передовое медицинское оборудование

Гарантия качества обслуживания
Хотите, мы Вам перезвоним?
Спасибо за обращение.
Ваша заявка принята. Наш специалист свяжется с Вами в ближайшее время
