Формула Фруктозы структурная химическая
Структурная формула
Истинная, эмпирическая, или брутто-формула: C6H12O6
Химический состав Фруктозы
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод | 12,011 | 6 | 40% |
| Na | Натрий | 22,99 | 12 | 6,7% |
| O | Кислород | 15,999 | 6 | 53,3% |
Молекулярная масса: 180,156
Фруктоза — (арабино-гексулоза, фруктовый сахар) — моносахарид, кетоноспирт, кетогексоза, изомер глюкозы.
В 1861 году Бутлеров синтезировал фруктозу конденсацией муравьиной кислоты в присутствии катализаторов: Ba(OH)2 и Ca(OH)2.
Физические свойства
Белое кристаллическое вещество, хорошо растворимое в воде. Температура плавления фруктозы ниже температуры плавления глюкозы. В 2 раза слаще глюкозы и в 4-5 раз слаще лактозы.
Химические свойства
В водных растворах фруктоза существует в виде смеси таутомеров, в которой преобладает β-D-Фруктопираноза и содержится, при 20 °C, около 20 % β-D-Фруктофуранозы и около 5 % α-D-Фруктофуранозы:
α-D-фруктофураноза — (2R,3S,4R,5R)-2,5-бис(гидроксиметил)оксолан-2,3,4-триол
α-L-фруктофураноза — (2S,3R,4S,5S)-2,5-бис(гидроксиметил)оксолан-2,3,4-триол
β-D-фруктофураноза — (2S,3S,4R,5R)-2,5-бис(гидроксиметил)оксолан-2,3,4-триол
β-L-фруктофураноза — (2R,3R,4S,5S)-2,5-бис(гидроксиметил)оксолан-2,3,4-триол
α-L-фруктопираноза — (2S,3R,4S,5S)-2-(гидроксиметил)-оксан-2,3,4,5-тетраол
β-D-фруктопираноза — (2S,3S,4R,5R)-2-(гидроксиметил)-оксан-2,3,4,5-тетраол
β-L-фруктопираноза — (2R,3R,4S,5S)-2-(гидроксиметил)-оксан-2,3,4,5-тетраол
Из водных растворов D-фруктоза кристаллизуется в пиранозной форме (D-фpyктoпиpaнозa) — бесцветных кристаллов, хорошо растворимых в воде, при низких температурах — в виде моно- и полугидратов, выше 21,4 °C — в безводной форме. По своим химическим свойствам фруктоза является типичной кетозой; восстанавливается с образованием смеси маннита и сорбита, с фенилгидразином она образует фенилозазон, идентичный фенилозазонам глюкозы и маннозы. В отличие от глюкозы и других альдоз, фруктоза неустойчива как в щёлочных, так и кислых растворах; разлагается в условиях кислотного гидролиза полисахаридов или гликозидов. Начальной стадией разложения фруктозы в присутствии кислот является дегидратация её фуранозной формы с образованием 5-метилолфурфурола, на чём основана качественная реакция на фруктозу в присутствии резорцина — проба Селиванова: Фруктоза окисляется KMnO
Фруктоза и пищевой сахар
Молекула сахарозы (пищевого сахара) состоит из двух простых сахаридов: глюкозы и фруктозы. В организме сахароза расщепляется на глюкозу и фруктозу. Поэтому по своему действию сахароза эквивалентна смеси 50 % глюкозы и 50 % фруктозы.
Нахождение
В живых организмах обнаружен исключительно D-изомер фруктозы. В свободном виде фруктоза присутствует почти во всех сладких плодах, а так же составляет до 80 % мёда, в качестве моносахаридного звена входит в состав сахарозы и лактулозы.
Фруктан — Википедия
Материал из Википедии — свободной энциклопедии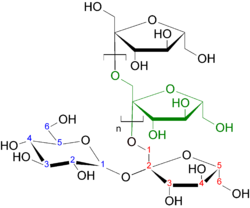 Структурная формула инулина, линейного фруктана с концевой α-D-глюкопиранозой, присоединённой связью 1→2
Структурная формула инулина, линейного фруктана с концевой α-D-глюкопиранозой, присоединённой связью 1→2Фруктан — полимер фруктозы. Каждая молекула фруктана состоит из множества молекул β-D-фруктозы и одной молекулы α-D-глюкозы, связанной с фруктозой через свой полуацетальный гидроксил. Таким образом, все фруктаны — невосстанавливающие полисахариды[1]. Особую группу составляют фруктаны с короткой цепью, называемые фруктоолигосахариды. Фруктаны можно обнаружить в таких продуктах питания как агава, артишок, спаржа, лук-порей, чеснок, лук (включая лук-шалот), якон, хикама и пшеница.
Фруктаны также содержатся в траве, и по одной из версий, могут быть одной из причин ламинита (воспаление копыт) у лошадей и других травоядных животных из семейства Equidae.
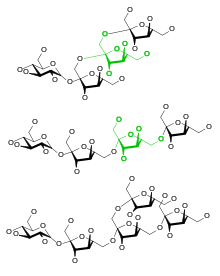
Фруктаны подразделяют на группы, в зависимости от типа связи между остатками фруктозы. Обычно связь осуществляется по первому (OH-1) или шестому (OH-6) гидроксилу и в соответствии с этим выделяют два основных типа фруктанов:
- 1-связанные: инулин, остатки фруктозы соединены связями β-2,1.
- 6-связанные: леван (или флеин), остатки фруктозы соединены связями β-2,6.
К третьей группе относятся граминан-подобные фруктаны: в них содержатся как β-2,1- так и β-2,6-связи[2].
Более сложные фруктаны образуются из кестотриозной цепи, в которой удлинение происходит с двух сторон. Как и в предыдущем случае, здесь выделяют два типа фруктанов:
- неоинулиновый тип: преобладают β-2,1-связи
- неолевановый тип: преобладают β-2,6-связи
Фруктаны служат запасающими полисахаридами. Они встречаются, например, у злаков (флеин и флеиноподобные фруктаны), а также астровых (инулин и инулиноподобные фруктаны). Заметным исключением является рис, который, будучи злаком, не синтезирует фруктаны [3]. Полагают, что у растений фруктаны синтезируются из сахарозы в вакуолях[1], однако этот процесс ещё слабо изучен. Помимо запасающей они могут выполнять осмотпротекторную функцию, а также являются биологическим антифризами, делая растение более холодоустойчивым[4][5].
Кроме растений, фруктаны могут синтезироваться рядом бактерий. Фруктан-синтезирующие штаммы есть среди Bacillus, Streptococcus, Pseudomonas, Erwinia, и Actinomyces. В основном они синтезируют β-2,6-связанные полисахариды — леваны. Синтез леванов происходит внеклеточно и осуществляется одним ферментом — левансахаразой (шифр КФ 2.4.1.10). При росте на среде, богатой сахарозой, бактерия выделяет этот фермент, который расщепляет сахарозу на глюкозу и фруктозу; при этом остаток фруктозы переносится на другую молекулы сахарозы. Вся глюкоза потребляется микроорганизмом, а фруктоза полимеризуется ферментом с образованием левана. После исчерпания глюкозы бактерия может расщепить полимер, используя ферменты леваназы и поглотить полученную фруктозу
| Топинамбур | 16,0—20,0 %[8] |
| Артишок испанский | 2,0—6,8 %[8] |
| Спаржа | 1,4—4,1 %[8] |
| Ядра ячменя (очень молодой) | 22 %[9] |
| Чеснок | 17,4 %[10] |
| Лук | 1,1—10,1 %[8] |
| Рожь (отруби) | 7 %[11] |
| Рожь (зерно) | 4,6—6,6 %[11] |
| Хлеб пшеничный (белый) | 0,7—2,8 %[8] |
| Пшеничная мука | 1—4 %[9] |
| Макароны | 1—4 %[8] |
- ↑ 1 2 Страсбургер, 2008, с. 220.
- ↑ Ende Wim Van den. Multifunctional fructans and raffinose family oligosaccharides (англ.) // Frontiers in Plant Science. — 2013. — Vol. 4. — ISSN 1664-462X. — DOI:10.3389/fpls.2013.00247. [исправить]
- ↑ Kawakami A., Sato Y., Yoshida M. Genetic engineering of rice capable of synthesizing fructans and enhancing chilling tolerance (англ.) // Journal of Experimental Botany. — 2008. — 7 March (vol. 59, no. 4). — P. 793—802. — ISSN 0022-0957. — DOI:10.1093/jxb/erm367. [исправить]
- ↑ POLLOCK C. J. TANSLEY REVIEW NO. 5 FRUCTANS AND THE METABOLISM OF SUCROSE IN VASCULAR PLANTS (англ.) // New Phytologist. — 1986. — September (vol. 104, no. 1). — P. 1—24. — ISSN 0028-646X. — DOI:10.1111/j.1469-8137.1986.tb00629.x. [исправить]
- ↑ Pollock C J, Cairns A J. Fructan Metabolism in Grasses and Cereals (англ.) // Annual Review of Plant Physiology and Plant Molecular Biology. — 1991. — June (vol. 42, no. 1). — P. 77—101. — ISSN 1040-2519. — DOI:10.1146/annurev.pp.42.060191.000453. [исправить]
- ↑ Vijn I., Smeekens S. Fructan: more than a reserve carbohydrate? (англ.) // Plant physiology. — 1999. — Vol. 120, no. 2. — P. 351—360. — PMID 10364386. [исправить]
- ↑ Rozen Ramona, Bachrach Gilad, Bronshteyn Moshe, Gedalia Itzhak, Steinberg Doron. The role of fructans on dental biofilm formation byStreptococcus sobrinus,Streptococcus mutans,Streptococcus gordoniiandActinomyces viscosus (англ.) // FEMS Microbiology Letters. — 2001. — February (vol. 195, no. 2). — P. 205—210. — ISSN 0378-1097. — DOI:10.1111/j.1574-6968.2001.tb10522.x. [исправить]
- ↑ 1 2 3 4 5 6 Shepherd S. J., Gibson P. R. Fructose malabsorption and symptoms of irritable bowel syndrome: guidelines for effective dietary management. (англ.) // Journal Of The American Dietetic Association. — 2006. — October (vol. 106, no. 10). — P. 1631—1639. — DOI:10.1016/j.jada.2006.07.010. — PMID 17000196. [исправить]
- ↑ 1 2 Slavin J. L. Mechanisms for the impact of whole grain foods on cancer risk. (англ.) // Journal Of The American College Of Nutrition. — 2000. — June (vol. 19, no. 3 Suppl). — P. 300—307. — PMID 10875601. [исправить]
- ↑ Muir, J.G. et al. Fructan and Free Fructose Content of Common Australian Vegetables and Fruit (англ.) // Journal of Agricultural and Food Chemistry (англ.)русск. : journal. — 2007. — Vol. 55. — P. 6619—6627. — DOI:10.1021/jf070623x.
- ↑ 1 2 Karppinen, Sirpa. Dietary fibre components of rye bran and their fermentation in vitro. Espoo 2003. VTT Publications 500. 96 p. + app. 52 p.[1]
- Sugar — Chemical, Biological and Nutritional Aspects of Sucrose. John Yudkin, Jack Edelman and Leslie Hough (1971, 1973). The Butterworth Group. ISBN 0-408-70172-2
- Зитте П. и др. Ботаника / Под ред. В. В. Чуба. — 35-е изд. — М.: Академия, 2008. — Т. 2. Физиология растений. — 495 с.
Углеводы: химические свойства, способы получения и строение
| Углеводы (сахара) – органические соединения, имеющие сходное строение, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3. |
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4 (на один атом кислорода меньше, чем рибоза).
По числу структурных звеньев
- Моносахариды — содержат одно структурное звено.
- Олигосахариды — содержат от 2 до 10 структурных звеньев (дисахариды, трисахариды и др.).
- Полисахариды — содержат n структурных звеньев.
Некоторые важнейшие углеводы:
| Моносахариды | Дисахариды | Полисахариды |
| Глюкоза С6Н12О6 Фруктоза С6Н12О6 Рибоза С5Н10О5 Дезоксирибоза С5Н10О4 | Сахароза С12Н22О11 Лактоза С12Н22О11 Мальтоза С12Н22О11 Целлобиоза С12Н22О11 | Целлюлоза (С6Н10О5)n Крахмал(С6Н10О5)n |
По числу атомов углерода в молекуле
- Пентозы — содержат 5 атомов углерода.
- Гексозы — содержат 6 атомов углерода.
- И т.д.
По размеру кольца в циклической форме молекулы
- Пиранозы — образуют шестичленное кольцо.
- Фуранозы — содержат пятичленное кольцо.
1. Горение
Все углеводы горят до углекислого газа и воды.
| Например, при горении глюкозы образуются вода и углекислый газ |
C6H12O6 + 6O2 → 6CO2 + 6H2O
2. Взаимодействие с концентрированной серной кислотой
Концентрированная серная кислота отнимает воду от углеводов, при этом образуется углерод С («обугливание») и вода.
| Например, при действии концентрированной серной кислоты на глюкозу образуются углерод и вода |
C6H12O6 → 6C + 6H2O
| Моносахариды – гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (группа альдегида или кетона) и несколько гидроксильных. |
Моносахариды являются структурными звеньями олигосахаридов и полисахаридов.
Важнейшие моносахариды
Глюкоза – это альдегидоспирт (альдоза).
Она содержит шесть атомов углерода, одну альдегидную и пять гидроксогрупп.
Глюкоза существует в растворах не только в виде линейной, но и циклических формах (альфа и бета), которые являются пиранозными (содержат шесть звеньев):
| α-глюкоза | β-глюкоза |
Химические свойства глюкозы
Водный раствор глюкозы
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
Качественная реакция на многоатомные спирты: реакция со свежеосажденным гидроксидом меди (II)
При взаимодействии свежеосажденного гидроксида меди (II) с глюкозой (и другими моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
Реакции на карбонильную группу — CH=O
Глюкоза проявляет свойства, характерные для альдегидов.
- Реакция «серебряного зеркала»
- Реакция с гидроксидом меди (II) при нагревании. При взаимодействии глюкозы с гидроксидом меди (II) выпадает красно-кирпичный осадок оксида меди (I):
- Окисление бромной водой. При окислении глюкозы бромной водой образуется глюконовая кислота:
- Также глюкозу можно окислить хлором, бертолетовой солью, азотной кислотой.
| Концентрированная азотная кислота окисляет не только альдегидную группу, но и гидроксогруппу на другом конце углеродной цепи. |
- Каталитическое гидрирование. При взаимодействии глюкозы с водородом происходит восстановление карбонильной группы до спиртового гидроксила, образуется шестиатомный спирт – сорбит:
- Брожение глюкозы. Брожение — это биохимический процесс, основанный на окислительно-восстановительных превращениях органических соединений в анаэробных условиях.
Спиртовое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
C6H12O6 → 2C2H5OH + 2CO2
Молочнокислое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
Маслянокислое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
- Образование эфиров глюкозы (характерно для циклической формы глюкозы).
Глюкоза способна образовывать простые и сложные эфиры.
Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила.
Например, α-D-глюкоза взаимодействует с метанолом.
При этом образуется монометиловый эфир глюкозы (α-O-метил-D-глюкозид):
| Простые эфиры глюкозы получили название гликозидов. |
В более жестких условиях (например, с CH3-I) возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами.
| Например, β-D-глюкоза реагирует с уксусным ангидридом в соотношении 1:5 с образованием пентаацетата глюкозы (β-пентаацетил-D-глюкозы): |
Получение глюкозы
Гидролиз крахмала
В присутствии кислот крахмал гидролизуется:
(C6H10O5)n + nH2O → nC6H12O6
Синтез из формальдегида
Реакция была впервые изучена А.М. Бутлеровым. Синтез проходит в присутствии гидроксида кальция:
6CH2=On → C6H12O6
Фотосинтез
В растениях углеводы образуются в результате реакции фотосинтеза из CO2 и Н2О:
6CO2 + 6H2O → C6H12O6 + 6O2
| Фруктоза — структурный изомер глюкозы. Это кетоноспирт (кетоза): она тоже может существовать в циклических формах (фуранозы). |
Она содержит шесть атомов углерода, одну кетоновую группу и пять гидроксогрупп.
Фруктоза – кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза.
В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы связаны с наличием кетонной и пяти гидроксильных групп.
При гидрировании фруктозы также получается сорбит.
| Дисахариды – это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой). |
Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом:
В молекуле сахарозы гликозидный атом углерода глюкозы связан из-за образования кислородного мостика с фруктозой, поэтому сахароза не образует открытую (альдегидную) форму.
| Поэтому сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании. Такие дисахариды называют невосстанавливающими, т.е. не способными окисляться. |
Сахароза подвергается гидролизу подкисленной водой. При этом образуются глюкоза и фруктоза:
C12H22O11 + 6H2O → C6H12O6 + C6H12O6
глюкоза фруктоза
Мальтоза С12Н22О11
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
| Мальтоза является восстанавливающим дисахаридом (одно из циклических звеньев может раскрываться в альдегидную группу) и вступает в реакции, характерные для альдегидов. |
При гидролизе мальтозы образуется глюкоза.
C12H22O11 + H2O → 2C6H12O6
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
| Полисахариды — это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов. |
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы.
Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (C6H10O5)n, но совершенно различные свойства.
Это объясняется особенностями их пространственного строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы:
Крахмал
Крахмалом называется полисахарид, построенный из остатков циклической α-глюкозы.
В его состав входят:
- амилоза (внутренняя часть крахмального зерна) – 10-20%
- амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 — 1000 остатков α-глюкозы (средняя молекулярная масса 160 000) и имеет неразветвленное строение.
Амилопектин имеет разветвленное строение и гораздо большую молекулярную массу, чем амилоза.
Свойства крахмала
- Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется:
Запись полного гидролиза крахмала без промежуточных этапов:
- Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
- Качественная реакция на крахмал: синее окрашивание с раствором йода.
Целлюлоза
Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
Свойства целлюлозы
- Образование сложных эфиров с азотной и уксусной кислотами.
Нитрование целлюлозы.
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании целлюлозы избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
Ацилирование целлюлозы.
При действии на целлюлозу уксусного ангидрида (упрощённо-уксусной кислоты) происходит реакция этерификации, при этом возможно участие в реакции 1, 2 и 3 групп ОН.
Получается ацетат целлюлозы – ацетатное волокно.
- Гидролиз целлюлозы.
Целлюлоза, подобно крахмалу, в кислой среде может гидролизоваться, в результате тоже получается глюкоза. Но процесс идёт гораздо труднее.
Поделиться ссылкой:
Галактоза — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 25 июня 2014; проверки требуют 22 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 25 июня 2014; проверки требуют 22 правки.| Галактоза | |||
|---|---|---|---|
 ( ({{{картинка2}}}) | |||
| Систематическое наименование | (2R,3S,4S,5R)-2,3,4,5,6-пентагидроксигексаналь (D-галактоза), (2S,3R,4R,5S)-2,3,4,5,6-пентагидроксигексаналь (L-галактоза) | ||
| Традиционные названия | галактоза, галактогексоза | ||
| Хим. формула | C6H12O6 | ||
| Молярная масса | 180,156 г/моль | ||
| Плотность | 1,723 г/см³ | ||
| Температура | |||
| • плавления | 167 °C | ||
| Растворимость | |||
| • в воде | 683,0 г/100 мл | ||
| Рег. номер CAS | 26566-61-0 | ||
| ChEBI | 28260 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Галакто́за (от греческого корня γάλακτ-, «молоко») — один из простых сахаров, моносахарид из группы гексоз, изомер глюкозы. Отличается от глюкозы пространственным расположением водородной и гидроксильной групп у 4-го углеродного атома. Содержится в животных и растительных организмах, в том числе в некоторых микроорганизмах. Один из основных и важных элементов, входящих в питание(пищу) грудных детей[1]. Входит в состав дисахаридов — лактозы и лактулозы. При окислении образует галактоновую, галактуроновую и слизевую кислоты. L-галактоза входит в состав полисахаридов красных водорослей. D-галактоза широко распространена в природе, входит в состав олигосахаридов (мелибиозы, рафинозы, стахиозы), некоторых гликозидов, растительных и бактериальных полисахаридов (камедей, слизей, галактанов, пектиновых веществ, гемицеллюлоз), в организме животных и человека — в состав лактозы, группоспецифических полисахаридов, цереброзидов, кератосульфата и др. В животных и растительных тканях D-галактоза может включаться в гликолиз при участии уридиндифосфат-В-глюкозо-4-эпимеразы, превращаясь в глюкозо-1-фосфат, который и усваивается. У человека наследственное отсутствие этого фермента приводит к неспособности утилизировать D-галактозу из лактозы и вызывает тяжёлое заболевание — галактоземию.
Галактоза может существовать в виде α- и β-галактозы
Циклические формы галактозы
α-D-галактофураноза — (2R,3R,4S,5S)-5-[(R)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
α-L-галактофураноза — (2S,3S,4R,5R)-5-[(S)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
β-D-галактофураноза — (2S,3R,4S,5S)-5-[(R)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
β-L-галактофураноза — (2R,3S,4R,5R)-5-[(S)-1,2-дигидроксиэтил)]-оксолан-2,3,4-триол
α-D-галактопираноза — (2R,3R,4S,5S,6R)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
α-L-галактопираноза — (2S,3S,4R,5R,6S)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
β-D-галактопираноза — (2S,3R,4S,5S,6R)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
β-L-галактопираноза — (2R,3S,4R,5R,6S)-6-(гидроксиметил)-оксан-2,3,4,5-тетраол
Биологический энциклопедический словарь / Гл. ред. М. С. Гиляров. — М.: Советская энциклопедия, 1986.
| Общие: | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Геометрия | |||||||||||||||
| Моносахариды |
| ||||||||||||||
| Мультисахариды | |||||||||||||||
| Производные углеводов | |||||||||||||||
Рибоза — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 февраля 2014; проверки требуют 15 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 февраля 2014; проверки требуют 15 правок.| D-рибоза | |
|---|---|
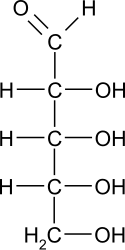 ( {{{картинка}}}) | |
| Систематическое наименование | (2R,3R,4R)-2,3,4,5-тетрагидроксипентаналь (D-рибоза) (2S,3S,4S)-2,3,4,5-тетрагидроксипентаналь (L-рибоза) |
| Традиционные названия | рибоза, рибопентоза |
| Рац. формула | C5H10O5 |
| Молярная масса | 150,13 г/моль |
| Плотность | 0.8 г/см³ |
| Температура | |
| • плавления | 90 °C |
| Растворимость | |
| • в воде | хорошо растворима в воде |
| Рег. номер CAS | 50-69-1 |
| ChEBI | 33942 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
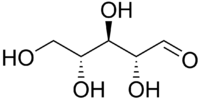 Ациклическая форма D-рибозы
Ациклическая форма D-рибозыРибо́за — моносахарид из группы пентоз, бесцветные кристаллы, легко растворимые в воде и имеющие сладкий вкус. Эпимер арабинозы. Открыта в 1905 году.
Рибоза, как и другие моносахариды, в растворах существует в виде равновесной смеси ациклической и циклических: пиранозной и фуранозной форм (аномерные α- и β-рибопиранозы и α- и β-рибофуранозы). Соотношение этих форм в растворе: β-рибопираноза (59%), α-рибопираноза (20%), β-рибофураноза (13%), α-рибофураноза (7%), ациклическая (0.1%).[1]
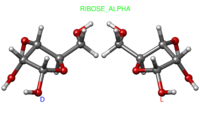 Альфа D,L-рибоза Альфа D,L-рибоза | 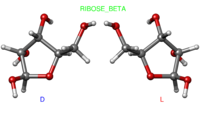 Бета D,L-рибоза Бета D,L-рибоза |
Рибоза восстанавливается водородом или амальгамой натрия до соответствующего альдита (рибита) и окисляется по альдегидной группе до соответствующей альдоновой (рибоновой) кислоты, способной циклизоваться в условиях синтеза в рибонолактон[2], с гидразинами образует озазоны.
Рибоза в форме β-D-рибофуранозы входит в состав рибонуклеиновой кислоты, нуклеозидов, нуклеотидов и других биологических важных веществ.
Рибоза является компонентом РНК и используется при генетической транскрипции. Производное β-D-рибозы — β-D-дезоксирибоза является компонентом ДНК. Также β-D-рибоза является компонентом АТФ и некоторых других веществ, участвующих в метаболизме.
Хиральность[править | править код]
Рибоза, входящая в состав биологических структур, обладает свойством хиральной чистоты : молекулы ДНК и РНК построены исключительно на «правой» рибозе[3].
- ↑ Kenneth N. Drew, Jaroslav Zajicek, Gail Bondo, Bidisha Bose, Anthony S. Serianni. 13C-labeled aldopentoses: detection and quantitation of cyclic and acyclic forms by heteronuclear 1D and 2D NMR spectroscopy // Carbohydrate Research. — 1998-02-01. — Т. 307, вып. 3–4. — С. 199–209. — DOI:10.1016/S0008-6215(98)00040-8.
- ↑ John D. Williams et al. D-Ribonolactone and 2,3-isopropylidene(d-ribonolactone). Organic Syntheses, Vol. 82, p.75 (2005).
- ↑ Никитин, Происхождение жизни, 2016, с. 177.
- Merck Index, 11th Edition, 8205
| Общие: | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Геометрия | |||||||||||||||
| Моносахариды |
| ||||||||||||||
| Мультисахариды | |||||||||||||||
| Производные углеводов | |||||||||||||||
Полисахариды — Википедия
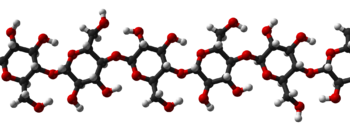

Полисахариды — высокомолекулярные углеводы, полимеры моносахаридов (гликаны). Молекулы полисахаридов представляют собой длинные линейные или разветвлённые цепочки моносахаридных остатков, соединённых гликозидной связью. При гидролизе образуют моносахариды или олигосахариды. У живых организмов выполняют резервные (крахмал, гликоген), структурные (целлюлоза, хитин) и другие функции.
Свойства полисахаридов значительно отличаются от свойств их мономеров и зависят не только от состава, но и от строения (в частности, разветвлённости) молекул. Они могут быть аморфными или даже нерастворимыми в воде.[1][2] Если полисахарид состоит из одинаковых моносахаридных остатков, он называется гомополисахаридом или гомогликаном, а если из разных — гетерополисахаридом или гетерогликаном.[3][4]
Природные сахариды чаще всего состоят из моносахаридов с формулой (CH2O)n, где n ≥3 (например, глюкоза, фруктоза и глицеральдегид)[5]. Общая формула большинства полисахаридов — Cx(H2O)y, где x обычно лежит между 200 и 2500. Чаще всего мономерами являются шестиуглеродные моносахариды, и в таком случае формула полисахарида выглядит как (C6H10O5)n, где 40≤n≤3000.
Полисахаридами обычно называют полимеры, содержащие больше десяти моносахаридных остатков. Резкой границы между полисахаридами и олигосахаридами нет. Полисахариды являются важной подгруппой биополимеров. Их функция в живых организмах обычно либо структурная, либо резервная. Запасным веществом высших растений обычно служит крахмал, состоящий из амилозы и амилопектина (полимеров глюкозы). У животных есть похожий, но более плотный и разветвленный полимер глюкозы — гликоген, или «животный крахмал». Он может быть использован быстрее, что связано с активным метаболизмом животных.
Целлюлоза и хитин — структурные полисахариды. Целлюлоза служит структурной основой клеточной стенки растений, это наиболее распространенное органическое вещество на Земле.[6] Она используется при производстве бумаги и тканей, и в качестве исходного сырья для производства вискозы, ацетилцеллюлозы, целлулоида и нитроцеллюлозы. Хитин имеет такую же структуру, но с азотсодержащим боковым ответвлением, увеличивающим его прочность. Он есть в экзоскелетах членистоногих и в клеточных стенках некоторых грибов. Он также используется во многих производствах, включая хирургические иглы. Полисахариды также включают каллозу, ламинарин, хризоламинарин, ксилан, арабиноксилан, маннан, фукоидан и галактоманнаны.
| Функция | Характеристика |
| Энергетическая | Основной источник энергии. Расщепляются до моносахаридов с последующим окислением до СО2 и Н2О. При расщеплении 1 г углеводов выделяется 17,6 кДж энергии. |
| Структурная | Входят в состав оболочек клеток и некоторых органелл. У растений полисахариды выполняют опорную функцию. |
| Запасающая | Накапливаются в тканях растений (крахмал) и животных (гликоген). Используются при возникновении потребности в энергии. |
| Защитная | Секреты, выделяющиеся разными железами, обогащены углеводами, например глюкопротеидами, защищающими стенки полых органов (пищевод, желудок, бронхи) от механических повреждений, проникновения вредных бактерий и вирусов. |
Свойства[править | править код]
Пищевые полисахариды — основные источники энергии. Многие микроорганизмы легко разлагают до глюкозы крахмал, но большинство микроорганизмов не могут переварить целлюлозу или другие полисахариды, такие как хитин и арабиноксиланы. Эти углеводы могут усваиваться некоторыми бактериями и протистами. Жвачные животные и термиты, к примеру, используют микроорганизмы для переваривания целлюлозы.
Даже при том, что эти сложные углеводы не очень легко усваиваемы, они важны для питания. Их называют пищевыми волокнами, эти углеводы улучшают пищеварение среди прочей пользы. Основная функция пищевых волокон — изменение природного содержимого желудочно-кишечного тракта, и изменение всасывания других нутриентов и химических веществ.[7][8] Растворимые волокна связываются с жёлчными кислотами в тонком кишечнике, растворяя их для лучшего усвоения; это в свою очередь понижает уровень холестерина в крови.[9] Растворимые волокна также замедляют всасывание сахара и уменьшают ответную реакцию на него после еды, нормализуют уровень содержания липидов в крови, и после ферментации в толстой кишке синтезируются в короткоцепочные жирные кислоты в качестве побочных продуктов с широким спектром физиологической активности (пояснение ниже). Хотя нерастворимые волокна и уменьшают риск диабета, механизм их действия до сих пор не изучен.[10]
Пищевые волокна считаются важными составляющими питания, и во многих развитых странах рекомендуется увеличивать их потребление.[7][8][11][12]
Крахмал[править | править код]
Крахмалы — полимеры глюкозы, в которых остатки глюкопиранозы образуют альфа-соединения. Они сделаны из смеси амилозы (15–20 %) и амилопектина (80–85 %). Амилоза состоит из линейной цепочки нескольких сотен глюкозных молекул, а амилопектин — разветвленная молекула, сделанная из нескольких тысяч глюкозных остатков (каждая цепочка из 24–30 глюкозных остатков — одна единица амилопектина). Крахмалы нерастворимы в воде. Они могут перевариться при разрыве альфа-соединений (гликозидные соединения). И у животных, и людей есть амилазы, поэтому они могут переварить крахмал. Картофель, рис, мука и кукуруза — главные источники крахмала в человеческом питании. Растения запасают глюкозу в виде крахмалов.
Гликоген[править | править код]
Гликоген служит вторым по значению долговременным энергетическим запасом в клетках животных и грибов, который откладывается в виде энергии в жировой ткани. Гликоген в первую очередь образовывается в печени и мышцах, но также может вырабатываться гликогеногенезом в головном мозге и желудке.[13]
Гликоген — аналог крахмала, глюкозного полимера в растениях, иногда его называют «животный крахмал»,[14] имеет схожую структуру с амилопектином, но больше разветвлен и компактен, чем крахмал. Гликоген — полимер, связанный гликозидными связями α(1→4) (в точках разветвления — α(1→6)). Гликоген находится в форме гранул в цитозоли/цитоплазме многих клеток и играет важную роль в глюкозном цикле. Гликоген формирует запас энергии, которая быстро пускается в обращение при необходимости в глюкозе, но он менее плотный и быстрее доступен в качестве энергии, чем триглицериды (липиды).
В гепатоцитах вскоре после еды гликоген может составлять до 8 процентов массы (у взрослых — 100—120 г).[15] Только гликоген, запасенный в печени, может быть доступен для других органов. В мышцах гликоген составляет 1-2 % массы. Количество гликогена, отложенного в теле — в особенности в мышцах, печени и эритроцитах[16][17][18] — зависит от физической активности, основного обмена и пищевых привычек, таких как периодическое голодание. Небольшое количество гликогена находится в почках, и ещё меньше в клетках глии в головном мозге и лейкоцитах. В матке также запасается гликоген во время беременности, чтобы рос эмбрион.[15]
Гликоген состоит из разветвленной цепочки глюкозных остатков. Он находится в печени и мышцах.
- Это энергетический запас для животных.
- Это основная форма углевода, отложенного в теле животного.
- Он нерастворим в воде. Йодом окрашивается в красный цвет.
- Он превращается в глюкозу в процессе гидролиза.
-

Схема гликогена в двумерном сечении. В сердцевине находится белок гликогенин, окруженный ответвлениями глюкозных остатков. Во всей глобулярной грануле может содержаться примерно 30 000 глюкозных остатков.[19]
Арабиноксиланы[править | править код]
Арабиноксиланы находятся и в главных, и во второстепенных стенках клеток растений, и они являются сополимерами двух пентозных сахаров: арабиноза и ксилоза.
Целлюлоза[править | править код]
Строительный материал растений формируется в первую очередь из целлюлозы. Дерево содержит, кроме целлюлозы, много лигнина, а бумага и хлопок — почти чистая целлюлоза. Целлюлоза — полимер повторяющихся глюкозных остатков, соединенных вместе бета-связями. У людей и многих животных нет энзимов разорвать бета-связи, поэтому они не переваривают целлюлозу. Определенные животные, такие как термиты, могут переварить целлюлозу, потому что в их пищеварительной системе присутствуют энзимы, способные переварить её. Целлюлоза нерастворима в воде. Не меняет цвет при смешивании с йодом. При гидролизе переходит в глюкозу. Это самый распространенный углевод в мире.
Хитин[править | править код]
Хитин — один из самых часто встречающихся натуральных полимеров. Он является строительным компонентом многих животных, к примеру экзоскелетов. Он разлагается микроорганизмами в течение долгого времени в окружающей среде. Его распад могут катализировать ферменты под названием хитиназы, которые секретируют такие микроорганизмы как бактерии и грибы, и производят некоторые растения. У некоторых из этих микроорганизмов есть рецепторы, которые расщепляют хитин до простого сахара. При нахождении хитина они начинают выделять ферменты, расщепляющие его до гликозидных связей, чтобы получить простые сахара и аммиак.
Химически хитин очень близок хитозану (более водорастворимое производное хитина). Он также очень похож на целлюлозу: это тоже длинная неразветвленная цепочка глюкозных остатков, но с добавочными группами. Оба материала придают организмам прочность.
Пектины[править | править код]
Пектины — совокупность полисахаридов, состоящих из а-1,4-связей между остатками D-галактопиранозилуроновой кислоты. Они есть во многих важнейших клеточных стенках и в недревесных частях растений.
Кислотные полисахариды — полисахариды, содержащие карбоксильные группы, фосфатные группы и/или группы серных сложных эфиров.
Бактериальные капсульные полисахариды[править | править код]
Патогенные бактерии обычно вырабатывают вязкий, слизистый слой полисахаридов. Эта «капсула» скрывает антигеновые белки на поверхности бактерии, которая иначе вызвала бы иммунный ответ и таким образом привела к разрушению бактерии. Капсульные полисахариды водорастворимые, зачастую кислотные, и у них есть молекулярная масса на уровне 100—2000 kDa. Они линейны и состоят из постоянно повторяющихся субъединиц от одного до шести моносахаридов. Существует огромное структурное многообразие; около двух сотен разных полисахаридов производится только одной кишечной палочкой. Смесь капсульных полисахаридов, либо конъюгируется, либо естественным путем используется как вакцина.
Бактерии и многие другие микробы, включая грибы и водоросли, часто секретируют полисахариды, чтобы прилипнуть к поверхностям для предотвращения пересыхания. Люди научились превращать некоторые такие полисахариды в полезные продукты, включая ксантановую камедь, декстран, гуаровая камедь, велановую камедь, дьютановую камедь и пуллулан.
Большинство из этих полисахаридов выделяют полезные вязкоупругие свойства, когда растворяются в воде на очень низком уровне.[20] Это позволяет использовать различные жидкости в ежедневной жизни, к примеру, в таких продуктах как лосьоны, очищающие средства и краски, вязкие в стабильном состоянии, но становятся намного более жидкие при малейшем движении и используются для размешивания или взбалтывания, чтобы наливать, вытирать или расчесывать. Это свойство называется псевдопластичностью; изучение таких материалов называется реология.
У водного раствора таких полисахаридов есть интересное свойство: если придать ему круговое движение, раствор сначала продолжает кружить по инерции, замедляя движение благодаря вязкости, а потом меняет направление, после чего останавливается. Этот разворот происходит благодаря упругости цепочек полисахаридов, которые после растяжения стремятся возвратиться в расслабленное состояние.
Мембранные полисахариды выполняют другие роли в бактериальной экологии и физиологии. Они служат барьером между клеточной стенкой и окружающим миром, посредником во взаимодействии хозяин-паразит, и образуют строительные компоненты биопленки. Эти полисахариды синтезируются из нуклеотидно-активированных предшественников (их называют нуклеотидные сахара) и, во многих случаях, все ферменты, необходимые для биосинтеза, собрания и транспортировки целого полимера закодированые генами, организованны в специальных группах с геномом организма. Липополисахарид — один из самых важных мембранных полисахаридов, играющий ключевую роль для сохранения структурной целостности клетки, а также являющийся важнейшим посредником во взаимодействии между хозяином и паразитом.
Недавно были найдены энзимы, которые образуют A-группу (гомополимерные) и B-группу (гетерополимерные) O-антигенов и определены их метаболические пути.[21] Экзополисахаридный альгинат — линейный полисахарид, связанный β-1,4-остатками D-маннуроновой и L-гулуроновой кислот, и ответственный за мукоидный фенотип последней стадии муковисцедоза. Локусы Pel и psl — две недавно обнаруженные генетические группы, которые также закодированы экзополисахаридами, и как выяснилось, являются очень важным составляющим биопленки. Рамнолипиды — биологические поверхностно-активные вещества, производство которых строго регулируется на транскрипционном уровне, но роль, которую они играют во время болезни, пока не изучена. Протеиновое гликозилирование, в частности пилин и флагеллин, стали объектом исследования нескольких групп начиная где-то с 2007 г., и как оказалось, они очень важны для адгезии и инвазии во время бактериальной инфекции.[22]
- ↑ Varki A., Cummings R., Esko J., Freeze H., Stanley P., Bertozzi C., Hart G., Etzler M. Essentials of glycobiology (неопр.). — Essentials of Glycobiology. — Cold Spring Harbor Laboratory Press; 2nd edition, 2008. — ISBN 0-87969-770-9.
- ↑ Varki A., Cummings R., Esko J., Jessica Freeze, Hart G., Marth J. Essentials of glycobiology (неопр.). — Essentials of glycobiology. — Cold Spring Harbor Laboratory Press (англ.)русск., 1999. — ISBN 0-87969-560-9.
- ↑ IUPAC Gold Book internet edition: «homopolysaccharide (homoglycan)».
- ↑ IUPAC Gold Book internet edition: «heteropolysaccharide (heteroglycan)».
- ↑ Matthews, C. E.; K. E. Van Holde; K. G. Ahern (1999) Biochemistry. 3rd edition. Benjamin Cummings. ISBN 0-8053-3066-6
- ↑ N.A.Campbell (1996) Biology (4th edition). Benjamin Cummings NY. p.23 ISBN 0-8053-1957-3
- ↑ 1 2 Dietary Reference Intakes for Energy, Carbohydrate, fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids (Macronutrients) (2005), Chapter 7: Dietary, Functional and Total fiber. (неопр.) (недоступная ссылка). US Department of Agriculture, National Agricultural Library and National Academy of Sciences, Institute of Medicine, Food and Nutrition Board. Архивировано 27 октября 2011 года.
- ↑ 1 2 Eastwood M., Kritchevsky D. Dietary fiber: how did we get where we are? (англ.) // Annu Rev Nutr (англ.)русск. : journal. — 2005. — Vol. 25. — P. 1—8. — DOI:10.1146/annurev.nutr.25.121304.131658. — PMID 16011456.
- ↑ Anderson JW; Baird P; Davis RH; and others. Health benefits of dietary fiber (англ.) // Nutr Rev (англ.)русск. : journal. — 2009. — Vol. 67, no. 4. — P. 188—205. — DOI:10.1111/j.1753-4887.2009.00189.x. — PMID 19335713.
- ↑ Weickert M. O., Pfeiffer A. F. Metabolic effects of dietary fiberand any other substance that consume and prevention of diabetes (англ.) // J Nutr (англ.)русск. : journal. — 2008. — Vol. 138, no. 3. — P. 439—442. — PMID 18287346.
- ↑ Dietary Benefits of Fucoidan from Sulfated Polysaccharides (неопр.) (недоступная ссылка). Дата обращения 16 августа 2017. Архивировано 16 августа 2017 года.
- ↑ Jones P. J., Varady K. A. Are functional foods redefining nutritional requirements? (англ.) // Appl Physiol Nutr Metab (англ.)русск. : journal. — 2008. — Vol. 33, no. 1. — P. 118—123. — DOI:10.1139/H07-134. — PMID 18347661. Архивировано 27 февраля 2012 года.
- ↑ Anatomy and Physiology. Saladin, Kenneth S. McGraw-Hill, 2007.
- ↑ Animal starch (неопр.). Merriam Webster. Дата обращения 11 мая 2014.
- ↑ 1 2 Campbell, Neil A.; Brad Williamson; Robin J. Heyden. Biology: Exploring Life (неопр.). — Boston, Massachusetts: Pearson Prentice Hall (англ.)русск., 2006. — ISBN 0-13-250882-6.
- ↑ Moses S. W., Bashan N., Gutman A. Glycogen metabolism in the normal red blood cell (англ.) // Blood (англ.)русск.. — American Society of Hematology (англ.)русск., 1972. — December (vol. 40, no. 6). — P. 836—843. — PMID 5083874. (недоступная ссылка)
- ↑ http://jeb.biologists.org/cgi/reprint/129/1/141.pdf
- ↑ Miwa I., Suzuki S. An improved quantitative assay of glycogen in erythrocytes (англ.) // Annals of Clinical Biochemistry (англ.)русск. : journal. — 2002. — November (vol. 39, no. Pt 6). — P. 612—613. — DOI:10.1258/000456302760413432. — PMID 12564847.
- ↑ Page 12 in: Exercise physiology: energy, nutrition, and human performance, By William D. McArdle, Frank I. Katch, Victor L. Katch, Edition: 6, illustrated, Published by Lippincott Williams & Wilkins, 2006, ISBN 0-7817-4990-5, ISBN 978-0-7817-4990-9, 1068 pages
- ↑ Viscosity of Welan Gum vs. Concentration in Water. Архивированная копия (неопр.) (недоступная ссылка). Дата обращения 2 октября 2009. Архивировано 18 июля 2011 года.
- ↑ Guo H., Yi W., Song J. K., Wang P. G. Current understanding on biosynthesis of microbial polysaccharides (англ.) // Curr Top Med Chem (англ.)русск. : journal. — 2008. — Vol. 8, no. 2. — P. 141—151. — DOI:10.2174/156802608783378873. — PMID 18289083.
- ↑ Cornelis P (editor). Pseudomonas: Genomics and Molecular Biology (англ.). — 1st. — Caister Academic Press (англ.)русск., 2008. — ISBN 978-1-904455-19-6.
| Общие: | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Геометрия | |||||||||||||||
| Моносахариды |
| ||||||||||||||
| Мультисахариды | |||||||||||||||
| Производные углеводов | |||||||||||||||
Мальтоза — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 февраля 2014; проверки требует 21 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 февраля 2014; проверки требует 21 правка.| Мальтоза | |
|---|---|
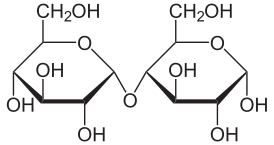 ( {{{картинка}}}) | |
| Систематическое наименование | 4-О-α-D-глюкопиранозил-D-глюкоза, |
| Традиционные названия | Мальтоза |
| Хим. формула | C12H22O11 |
| Состояние | Белый порошок или кристаллы |
| Молярная масса | 342,32 г/моль |
| Плотность | 1.54 г/см³ |
| Температура | |
| • плавления | 160–165 °C (Дигидрат) 102-103 °C (Моногидрат) |
| Растворимость | |
| • в воде | 1.080 г/100 мл |
| Рег. номер CAS | 69-79-4 |
| PubChem | 439186 |
| Рег. номер EINECS | 200-716-5 |
| SMILES | |
| InChI | 1S/C12h32O11/c13-1-3-5(15)6(16)9(19)12(22-3)23-10-4(2-14)21-11(20)8(18)7(10)17/h4-20H,1-2h3/t3-,4-,5-,6+,7-,8-,9-,10-,11?,12-/m1/s1 |
| RTECS | LZ6600000 |
| ChEBI | 17306 |
| ChemSpider | 388329 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Мальто́за (от англ. malt — солод) — солодовый сахар, 4-О-α-D-глюкопиранозил-D-глюкоза, природный дисахарид, состоящий из двух остатков глюкозы; содержится в больших количествах в проросших зёрнах (солоде) ячменя, ржи и других зерновых; обнаружен также в томатах, в пыльце и нектаре ряда растений.
Биосинтез мальтозы из β-D-глюкопиранозилфосфата и D-глюкозы известен только у некоторых видов бактерий. В животном и растительном организмах мальтоза образуется при ферментативном расщеплении крахмала и гликогена (см. Амилазы).
Мальтоза легко усваивается организмом человека. Расщепление мальтозы до двух остатков глюкозы происходит в результате действия фермента a-глюкозидазы, или мальтазы, которая содержится в пищеварительных соках животных и человека, в проросшем зерне, в плесневых грибах и дрожжах. Генетически обусловленное отсутствие этого фермента в слизистой оболочке кишечника человека приводит к врождённой непереносимости мальтозы — тяжёлому заболеванию, требующему исключения из рациона мальтозы, крахмала и гликогена или добавления к пище фермента мальтазы.
α-Мальтоза — (2R,3R,4S,5R,6R)-5-[(2R,3R,4S,5R,6R)-2,3,4-тригидрокси-6-(гидроксиметил)оксанил]окси-6-(гидроксиметил)оксан-2,3,4-триол
β-Мальтоза — (2S,3R,4S,5R,6R)-5-[(2R,3R,4S,5R,6R)-2,3,4-тригидрокси-6-(гидроксиметил)оксанил]окси-6-(гидроксиметил)оксан-2,3,4-триол
Мальтоза легко растворима в воде, имеет сладкий вкус. Молекулярная масса мальтозы — 342,32. Температура плавления мальтозы — 102°C (безводная).

Мальтоза является восстанавливающим сахаром, так как имеет незамещённую полуацетальную гидроксильную группу.
При кипячении мальтозы с разбавленной кислотой и при действии фермента мальтоза гидролизуется (образуются две молекулы глюкозы C6H12O6).
C12h32O11+h3O→2C6h22O6.{\displaystyle {\mathsf {C_{12}H_{22}O_{11}+H_{2}O\rightarrow 2C_{6}H_{12}O_{6}}}.}
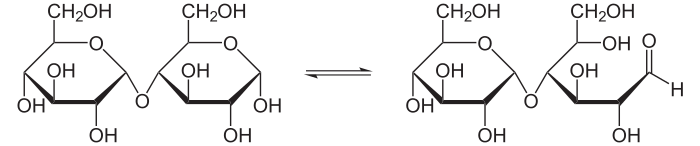 Баланс между циклической и открытой формой мальтозы
Баланс между циклической и открытой формой мальтозы- Химия углеводов. — М.:, 1967.
- Харрис Г. Основы биохимической генетики человека. Пер. с англ. — М.:, 1973.

 (
(