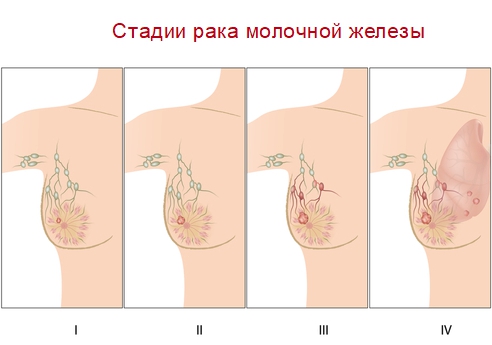
прогноз развития в послеоперационном рубце после мастэктомии
Рецидив рака молочной железы – это повторное поражение тканей организма раковыми клетками. После прохождения курса медикаментозного и хирургического вмешательства возможно повторное появление симптомов онкологического заболевания. Повторное течение болезни становится более агрессивным и отрицательно сказывается на состоянии пациентки. Учитывается несколько факторов при прогнозировании повторения болезни. Вероятность повторного развития зависит от разновидности опухоли, стадии заболевания, способов лечения.
Опыт работы врачей-онкологов помог достичь хороших результатов при лечении рака молочной железы и уменьшить динамику смертности в результате этого заболевания. Несмотря на успехи медицины, наблюдаются рецидивы после процедуры мастэктомии (радикальный метод, предусматривающий удаление молочной железы хирургическим путём).
Если врачи обнаруживают раковые клетки через месяц после лечения, это считается неудачным лечением. Нередки случаи, когда спустя долгий период времени после выздоровления рак диагностируется в другой молочной железе. Данная ситуация – не повторный, а первичный рак молочной железы.
Врачи рассматривают три разновидности рецидивов.
Местный
Такой вид предусматривает повторное появление раковых клеток на прежней молочной железе. Проявляются в ранние сроки и обладают большими размерами. Не исключено, что рубец от предыдущей операции станет очагом опухоли. Причиной вторичного появления раковых клеток врачи считают недостаточную эффективность лечения первичного заболевания, когда не все раковые клетки оказались уничтожены.
Хирургическое вмешательство без проведения гормональной терапии, после которого остаются элементы поражённой кожи и жировой ткани, делает возможным повторение рака груди в послеоперационном рубце. При щадящем лечении, когда молочную железу удаляют частично или не трогают вообще, а подвергают лучевой терапии, частота повторного поражения выше. Для определения наличия раковых клеток проводят биопсию материала, взятого из рубца. Локальные типы новообразования преимущественно возникают в первые 5 лет, с частотой 75%. По данным исследований, второй год последующий за мастэктомией, имеет максимальную частоту рецидивов.

Если вовремя не распознать рак и не принять меры, направленные на уничтожение локализованного очага повторного поражения, течение заболевания осложнится метастазами в другие органы.
После проведённых мероприятий для устранения очагов болезни женщинам рекомендуется самостоятельно осматривать, прощупывать грудь, не игнорировать визиты к врачам. Чтобы определить возвращение онкологии, больной необходимо знать внешние признаки проявления болезни.
Симптомы
О появлении местного рецидива свидетельствуют признаки:
- покраснение;
- воспаление кожи на пролеченной молочной железе;
- эрозии рядом с соском;
- появление узлов под послеоперационным рубцом, которые не доставляют неприятности;
- выделения из груди;
- изменение цвета кожного покрова;
- уплотнение, утолщение кожи на месте операции.
Следует насторожиться, если проявляется анемия, повышение температуры тела, отсутствие аппетита, снижение веса, повышенная утомляемость. При обнаружении любого из симптомов следует немедленно обратиться к врачу, чтобы он выслушал жалобы, составил клиническую картину, назначил анализы для определения вероятности возобновления очагов опухоли.
При выборе лечения вторичного рака учитывают ряд нюансов: пожелания женщины, размер поражённого участка, ранее использованные методы, тип рецидива.
Выбор стратегии борьбы и прогнозирование
При местном рецидиве, при условии, что хирургическое вмешательство ранее не проводилось, часто выбор падает на удаление молочной железы с совмещением последующей лекарственной терапией. При вторичном возникновении заболевания с большим очагом поражения органосохраняющие мероприятия не проводятся во избежание метастазирования.
В случае небольшого размера повторной опухоли, врачи не исключают проведение второго органосохраняющего лечения.
Если операция уже проводилась, при повторном заболевании удаляется сама опухоль и расположенные поблизости здоровые участки. Для исключения вероятного сохранения поражённых клеток проводится дополнительное комплексное лечение, постоперационная терапия, которую женщина должна проводить, находясь дома.
Повторная лучевая терапия противопоказана, предполагается использование гормональной и химиотерапии.
Наряду с мероприятиями, направленными на уничтожение клеток новообразования, принимается ряд мер для поддержания психологического состояния женщины.
Локальный тип вторичного возникновения рака груди позволяет делать оптимистичные прогнозы: около 75% женщин имеют шансы на полноценную жизнь в течение 5 и более лет. Распознание болезни на первой стадии может повысить шансы на полное выздоровление.
Регионарный
Регионарным рецидивом называют состояние, когда раковые клетки распространяются в подрёберные и грудные ткани, мышцы груди, в лимфатические узлы грудного и шейного отдела. Такой вид считается агрессивным, и частота его возникновения составляет 5%. При регионарном типе вторичного поражения присутствует угроза распространения раковых клеток в другие органы через лимфатические узлы или кровеносные сосуды. Избежать такого исхода удастся при помощи раннего диагностирования.
Симптомы
Симптомы регионарного поражения – наличие боли из-за врастания опухолевых клеток в грудину, уплотнения или шишки в подмышечном, подключичном и шейном отделе. Отсутствие аппетита, общая слабость организма, частая утомляемость, повышенная температура должны стать сигналом для посещения маммолога, а потом – онколога.
Выбор стратегии борьбы и прогнозирование
Лечение регионарного рецидива требует больших усилий, целесообразным является использование нескольких способов параллельно: хирургическое удаление участков поражения, гормональная, лучевая и химиотерапия. Цель комплексной терапии – уничтожение всех раковых клеток и недопущение распространения по организму.

Прогнозирование течения болезни производится с учётом возраста, общего состояния организма после первичной мастэктомии и последующей адъювантной (послеоперационной) терапии, количества заражённых лимфоузлов.
Отдалённый
Под термином «отдалённый рецидив» принято считать возникновение метастазов отдалённых органов. Шансов на полное выздоровление при такой разновидности рецидива мало. Поражение раковыми клетками происходит через лимфатические узлы, кровеносные сосуды, по которым они попадают в любой орган, поражая даже кости. Зоной поражения может стать мозг, лёгкие, брюшная часть, печень, грудная часть, здоровые ткани.
Описание признаков рецидивов
Головные боли, долгий кашель, длительное, но бесполезное лечение боли в спине и костях относят к симптомам развития метастазов. Изменение состояния и цвета кожи (мраморный оттенок) сигнализирует о том, что в организме присутствуют раковые клетки. На фоне субъективных ощущений женщины необходим внеплановый визит к врачу для уточнения диагноза.
Выбор стратегии борьбы и прогнозирование
Отдалённая локализация не предусматривает хирургического вмешательства, так как отмечается обширное метастазирование и ослабленный организм в результате первичного лечения. Для продления жизни женщины проводят параллельный курс терапии гормонами, химическими препаратами, облучением.
Выживаемость в данном случае снижается, так как полностью уничтожить рак не удаётся. Очаги будут возникать в других органах.
Как часто развивается вторичный рак
Возвращение болезни возможно, если после мастэктомии клетки рака остаются на прежнем месте. Через какое-то время оставшаяся клетка начинает развиваться, и врачи отмечают возвращение болезни.
Если в борьбе с раком молочной железы не использовались иные методы, кроме мастэктомии, у 40% женщин происходит повторение болезни первые 5 лет. Двухлетний период после операции считается самым рискованным в случае, когда, кроме радикального метода борьбы, не использовались другие.
Статистика показывает, что частота рецидивов при лечении рака груди на первой стадии выше, чем на последующих стадиях. Причина: методы борьбы с раком первой стадии используются щадящие, исключающие проведение гормональной терапии и удаление молочной железы.
Уровень смертности и повторное возникновение в первый десятилетний постоперационный период – высокий.
Вероятность развития вторичной опухоли зависит от нескольких факторов: радикальность методов, наличие или отсутствие гормональной терапии, стадия болезни, на которой проводилось лечение.
Рак молочной железы считают вылеченным, если за 5 лет не проявлялось признаков заболевания. К сожалению, злокачественная опухоль груди может вернуться и через 20 лет.
Чем обусловлено повторное развитие болезни
Методы, применяемые для лечения рака: гормональная терапия, облучение, химиотерапия не всегда оказываются эффективными. Известны случаи, когда годами спящие раковые клетки просыпаются и начинают размножаться. Существует ряд факторов, по которым можно предугадать вероятность повторения болезни:
- Объём новообразования. Тем выше возможность возвращения болезни, чем больше по размеру первичная опухоль.
- Если лимфатические узлы женщины поражены раковыми клетками при первом случае, риск рецидива возрастает.
- Врачи оценивают злокачественность по нескольким критериям. Скорость, с которой делятся клетки опухоли. Чем быстрее делятся клетки новообразования, тем злокачественнее опухоль. Определение типа опухоли путём гистологического анализа. Выявляют два гистологических типа: инвазивная протоковая карцинома агрессивнее, чем инвазивная дольковая карцинома. Агрессивность первой обуславливается тем, что раковые клетки по млечным протокам распространяются на близлежащие ткани. Способность раковых клеток менять форму, размеры. Учитывая три критерия, специалисты выделяют высокодифференцированный и низкодифференцированный рак. Первый вид менее агрессивен, ему не свойственны частые случаи рецидива. Низкодифференцированный рак отличается агрессивным течением болезни и частыми повторами.


- Стадия болезни, на которой проводилось лечение. После лечения рака первой стадии шансов исключить рецидив больше, чем на других этапах. Обуславливается это тем, что на последующих этапах территория поражения больше и проведение эффективного лечения оказывается затруднительным.
- После операции за состоянием здоровья женщины тщательно наблюдают. Для выявления предпосылок возвращения болезни проводят анализы на выявление протеина HER2 – показателя развития злокачественной опухоли.
- Если после лечения в опухолевых сосудах наблюдаются раковые клетки, вероятность повторной вспышки опухоли повышается.
- Риск повторного случая заболевания – выше, если в анализах найден прогестерон и эстроген.
- Повышенный уровень белка Ki-67 свидетельствует о предраковом состоянии.
Группы риска
Выделяется три группы риска, предрасположенных к рецидиву в большей или меньшей степени:
- Риск считается низким, если соблюдаются условия: опухоль размером менее 2 сантиметров, в соответствии с гистологическим анализом рак причислен к высокодифференцированному, клетки не внедрились в лимфатический узел, для уничтожения первичной злокачественной опухоли мастэктомия применялась параллельно с комплексной терапией, отсутствие в анализах наличия белка – признака злокачественной опухоли, женщина – молодая.
- К умеренному риску причисляют в следующих случаях: опухоль превышает 2 сантиметра, дифференцированность – низкая или средняя, в близлежащих сосудах присутствуют опухолевые клетки, анализ выявил наличие гена – маркера рака молочной железы, молодой возраст женщины.
- К группе высокого риска причисляют по следующим условиям: поражено от 1 до 3 лимфатических узла, присутствует маркер злокачественной опухоли – Her2, опухолевыми клетками поражены 4 лимфатических узла, высокая скорость размножения злокачественного образования, обнаружение предыдущего очага на поздних стадиях и его лечение с помощью единственного способа.


Степень риска повторного появления раковых клеток зависит от стратегии лечения. После проведения процедуры мастэктомии без сопутствующего комплекса мероприятий вероятность возобновления болезни достигает до 60%. Проведённое радиолечение позволяет снизить данный показатель до уровня 20-40%. Включение лучевой терапии в курс лечения способствует снижению рецидивов до 10%.
Профилактика
Соблюдение и своевременное проведение профилактических мероприятий способно снизить риск повторного возникновения болезни. Курс химиотерапии сразу после операции способен снизить риск последующего развития онкологического заболевания. Постоперационная гормонотерапия также способствует снижению риска рецидива молочной железы на 30%, что повышает уровень выживаемости пациенток.
Необходимо ограничить выработку эстрогена, способствующего росту раковых клеток. Для этого женщине прописывают специальные лекарства, подавляющие его выработку. Недопустим резкий набор массы и потеря в весе. Показания весов должны находиться на одном уровне. Здоровый образ жизни, исключающий употребление алкогольных напитков, курение. Прохождение маммографии и визит к маммологу периодичностью в 6 месяцев повышает возможность выявления повторных очагов поражения.
Регулярное самостоятельное прощупывание молочной железы поможет выявить возобновление болезни на раннем этапе. Исключение хронических заболеваний, способствующих ослаблению защитных сил организма. Ограничение в приёме гормональных препаратов. Доказано, что беременность, грудное вскармливание снижает онкологический риск. Включение витаминных комплексов, активизирующих работу иммунитета.
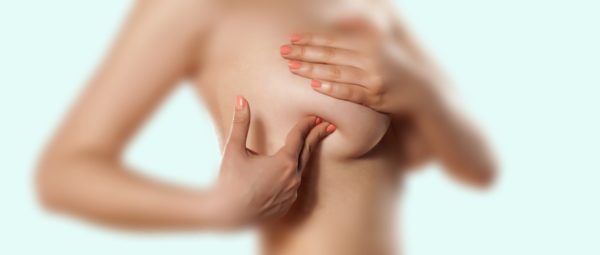

Самообследование молочных желёз
Методы диагностирования
На ранних этапах раковые клетки никак не проявляются, что затрудняет диагностирование. Женщинам с перенесённым раком груди положен регулярный самостоятельный осмотр молочных желёз. Если при проведении осмотра что-то настораживает, обязателен визит к маммологу.
Врач выносит вердикт о возвращении болезни после изучения клинической картины, осмотра пациентки, проведённой маммографии. Уточнить диагноз помогут различные виды томографии, сканирование, рентген, а также пункция и биопсия материала для гистологического анализа. Результаты биопсии помогут определить рецидив ли это, либо новое онкологическое заболевание.
Раннее диагностирование предотвратит осложнения течения болезни, так как переход от начальной стадии до последней у молодых женщин протекает в кратчайшие сроки.
Препараты нового поколения для лечения рака груди
Медицина не стоит на месте, фармацевты изобрели действенные лекарства для лечения рака молочной железы. Принцип действия таких препаратов такой: таргетные (от слова target – цель) препараты целенаправленно уничтожают раковые клетки или останавливают их последующую активность. Применение подобных препаратов не исключает другие виды терапии.
Прогнозирование исхода заболевания
При повторении злокачественного новообразования молочной железы делать прогноз трудно, так как на течение болезни влияет ряд факторов: возраст пациентки, физические показатели организма, тип рецидива, образ жизни.
Так, после лечения местного типа рецидивирующего рака, при условии эффективной терапии, прогнозы – обнадёживающие, уровень выживаемости до 5 лет составляет 60%. При отдалённом типе повторения болезни пациентки проживают только 3 года.
признаки, стадии развития, симптомы и прогнозы

За злокачественной меланомой закрепилась репутация полной непредсказуемости, тем не менее, в сравнении с другими раковыми процессами достаточно много известно про закономерности её прогрессирования.
Как выглядит рецидив меланомы?
Рецидивное новообразование отличается от первичной меланомы не столько внешним видом, сколько общим объемом поражения. Нередко вторичные образования очень похожи на ранее удаленное материнское, только их много больше, они могут быть крупнее или мельче.
В отечественной онкологии различают четыре вида рецидивов меланомы по классификации Вагнера:
- местные — опухоль располагается точно в зоне первичной операции;
- транзитные метастазы или сателлиты — рядом с рубцом, но не ближе 2 сантиметров, могут локализоваться не только в коже, но и в подкожно в клетчатке;
- регионарные метастазы — поражение злокачественным процессом лимфатических узлов вблизи зоны операции;
- отдалённые метастазы — вторичные меланомные опухоли в других органах и тканях.
У пациента могут быть рецидивы любого вида и в любом наборе, и все сразу, что неудивительно для столь агрессивной опухоли.
Причины рецидива меланомы
Предполагается, что источником развития рецидивной или метастатической опухоли становится злокачественная клетка, сохранившаяся в кровеносном или лимфатическом сосуде. На вероятности возврата болезни сказывается агрессивная биология меланомной клетки и её способность к длительному выживанию.
Замечено, что рецидивный процесс характерен для молодых людей от 30 до 50 лет, а сроки прогрессирования ассоциированы с полом. К примеру, поражение регионарных лимфоузлов у женщин случается на первом году после удаления меланомы, у мужчин — на втором-третьем, отдаленные метастазы у мужчины вероятны в первые 3 года после лечения, у женщины — после 3 лет.
Толщина первой опухоли коррелирует с частотой прогрессирования, при толщине более 2 мм у 8–9 пациентов из десятка скорее всего появятся метастазы в лимфоузлах. В клинических исследованиях разработан стандартный подход к расстоянию от опухоли до линии разреза в зависимости от толщины опухолевого узла, так не менее полсантиметра отступают при минимальной высоте, при более чем 2-миллиметровой толщине узелка от него отходят на 2 сантиметра.
Как недавно выяснили, на вероятности рецидивирования мало отражается объём первичной операции, но при недостаточном объеме иссечения, когда в краях удаленных тканей при гистологическом исследовании находят злокачественные клетки, не позже 8 недель выполняется повторная операция или проводится облучение с профилактической лекарственной терапией.
Места локализации
Две трети рецидивов — это метастазы, одна треть — узловые образования в зоне первой операции. Локализация материнской опухоли сказывается на судьбе пациента:
- у каждого третьего, оперированного по поводу меланомы кожи головы и шеи, развиваются опухоли в рубце, причём у женщин беда случается в первый год после лечения;
- транзитные метастазы имеют самую большую процентную долю в группе меланом конечности, такой вариант прогрессии у женщин развивается через пятилетку после иссечения, а в мужской популяции — на втором и третьем году после операции;
- при исходном поражении кожи ноги чаще всего, у семи из десяти обнаруживают вторичные опухоли в лимфоузлах, у женщин в ближайший год, у мужчин чуть позже;
- первичный процесс на туловище у каждого четвёртого осложняется отдаленными метастазами.
Признаки и симптомы меланомы
Признаки рецидивного образования в коже и мягких тканях не отличаются от таковых при первичной опухоли, к ним применим тот же диагностический алгоритм: асимметричность и неровность окраски, неровность краёв и нестабильность состояния. Размеры весьма вариабельны — от крошечных до гигантских «с голову младенца».
Симптомы метастазов зависят от места расположения, так при поражении легких может быть кашель с одышкой, при метастазировании в головной мозг — нарушение зрения, головные боли, рвота, судороги.
Регионарное метастазирование проявляется увеличением пакета лимфоузлов, с последующим прорастанием опухоли в мягкие ткани и блокировкой рядом проходящих сосудов, что осложняется отёком конечности.
Клинические исследования доказали, что выявление прогрессирования болезни до появления симптомов существенно улучшает перспективы на жизнь. Течение болезни всегда индивидуально, поэтому наблюдение после лечения должно опираться на биологические характеристики злокачественной опухоли. В Европейской клинике делается всё для раннего обнаружения и предотвращения проблем со здоровьем.
Группы рецидива
В 1985 году отечественный онколог Анисимов предложил для удобства описания клинической картины подразделять рецидивные опухоли на шесть групп:
- Первая — круглые и немногочисленные образования, часто вне рубца и преимущественно подкожно — в жировой клетчатке, нередко подпадают под критерии «транзитного» метастаза по Вагнеру.
- Вторая — множественная неправильной формы кожная и подкожная инфильтрация, сопровождающая сосуды и нервы, предполагается, что внешнюю картину рецидива формируют опухолевые клетки, прижившиеся в мелких сосудиках.
- Третья — непосредственно связанные с зоной операции узелки, разросшиеся из оставшихся в коже злокачественных клеток.
- Четвёртая — полициклические множественные образования.
- Пятая — множество выбухающих узелков, нередко на ножке, как грибы сморчки.
- Шестая — комбинация всех пяти вариантов.
Классификация в клинической практике используется редко, потому что оценка результатов лечения базируется исключительно на размерах узлов, а не на внешнем виде.

Частота возникновения
При любом виде и размере меланомы самый частый вариант прогрессии после операции — метастазы в другие органы почти у 60% больных.
Самый опасный период — первые три года после хирургического вмешательства, но на первом году у 60% более вероятны метастазы в регионарных лимфоузлах. При 1 и 2 стадии частота поражения лимфоузлов невысока — у каждого пятого, и совсем редко — менее 5% поражается послеоперационный рубец.
Из-за развития рецидивов заболевания только 60% больных живет больше пятилетки, но болезнь способна вернуться и через 15 лет — у 7%, и после 25 лет — у 10%. У каждого пятого с неважным индивидуальным прогнозом, тем не менее, в ближайшие 5 лет рецидива не возникает.
Диагностика
Обследование проходит аналогично диагностике первичного процесса. Особенность диагностики прогрессирования — четкое соблюдение графика регулярных осмотров, что позволяет выявить процесс в самом начале и до появления клинических симптомов.
В европейских странах рекомендуют посещать онколога каждые 2 месяца на протяжении первого года после операции, на втором году — ежеквартально, и далее наблюдаться, не сбавляя интенсивности, поскольку чаще всего рецидивы случаются в первые три года.
Ранняя диагностика рецидива меланомы сегодня объективная реальность. В каждом клиническом случае в Европейской клинике используется индивидуальная программа диагностического поиска, исключающая как избыточность обследования, так и его недостаточность.
Лечение
Лечение местного рецидива в рубце, транзитных метастазов и изменённых лимфатических узлов аналогично тактике при первичной опухоли — оптимальна операция в том числе с пластическим закрытием большого дефекта тканей.
Адъювантное лекарственное лечение после операции — норма, из лекарств используется то, что ранее не применялось для профилактики, правда выбор небольшой: альфа-интерферон и ипилимумаб.
При метастазах в другие органы встает вопрос о лекарственной терапии, и в первой линии прибегают к иммуно-онкологическим препаратам в сочетании с таргетными лекарствами при наличии мутации генов.
Выбор препаратов большой, поэтому при отсутствии результата или прогрессировании на фоне лечения во второй линии прибегают к ранее не использованным лекарствам. Химиотерапия при рецидиве меланомы используется в последнюю очередь совсем не из-за выраженных побочных реакций, проблема в невысоком результате.

Профилактика
Не существует специфической профилактики, воздействующей на факторы риска прогрессирования, но избегание солнечной инсоляции играет позитивную роль и в предотвращении рецидивирования.
Аналогичную задачу решает и визуальный контроль невусов у переболевшего меланомой пациента с обязательным соблюдением графика медицинских осмотров.
Чем опасен рецидив
Рецидив при меланоме — это не только появление злокачественного образования в рубце, но и метастазы. Чаще всего ими поражаются лимфатические узлы, легкие, кожа, головной мозг и печень. Возможность удаления рецидивного образования открывает перспективы на долгую жизнь, если операция технически невыполнима, то настоящее и будущее будет занято лекарственной терапией.
Выживаемость при множественных органных метастазах не превышает полугода, результаты лекарственной терапии оставляют желать лучшего даже при использовании инновационных иммуноонкологических препаратов, которые редко обещают более двух лет жизни.
Прогноз
Ежегодно меланома диагностируется в среднем у 15 человек из каждых ста тысяч взрослых, умирает примерно 3 больных, причем при достаточно стабильной смертности в последнюю четверть века мужчины стали гибнуть чаще. Пол многое определяет в прогнозе заболевания при прочих равных условиях, но молодые переживают заболевание с меньшими трудностями.
Вероятность смерти при позднем рецидиве многократно ниже, чем при раннем. Раннее выявление прогрессирования обещает лучшие результаты лечения.
Крайне сложно прогнозировать течение меланомы, потому что даже распространенный процесс не считается безусловно смертельным, это злокачественное заболевание не часто оправдывает ожидания. Не гадайте «быть или не быть», обратитесь к специалистам при наличии проблем, а лучше до их появления — мы всегда поможем.
Запись на консультацию круглосуточно
Список литературы
1. Семилетова Ю.В., Анисимов В.В., Вагнер Р.И. /Лечение больных первичной меланомой кожи. Современное состояние проблемы // Сибирский онкологический журнал. 2010. № 4.
2. Семилетова Ю.В., Анисимов В.В., Лемехов В.Г. и соавт./Факторы риска рецидивов после радикального лечения меланомы кожи//Сибир.онко.журн.; 2012. № 2 (50)
3. Строяковский Д. Л., Абрамов М. Е., Демидов Л. В. и соавт. /Практические рекомендации по лекарственному лечению меланомы кожи // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2018 (том 8)
4. de Vries E., Bray F.I., Coebergh J.W., Parkin D.M. /Changing epidemiology of malignant cutaneous melanoma in Europe 1953–1997: rising trends in incidence and mortality but recent stabilizations in western Europe and decreases in Scandinavia// Int J Cancer 2003; 107.
местный рецидив рака молочной железы, признаки и причины рецидива РМЖ

Рецидив рака молочной железы в российской онкологии трактуется несколько иначе. Иностранные клинические онкологи рецидивом считают возвращение рака в любом варианте, будь то новообразование в рубце после операции на молочной железе или множественные метастазы. В отечественной онкологии принято разделять рецидив и метастазирование.
Виды рецидивов
Рецидивы классифицируют:
- изолированный или локальный, то есть возникший в послеоперационной зоне: в рубце на грудной стенке после удаления молочной железы, в оставшейся части молочной железе, в тканях грудной стенки на стороне оперированной молочной железы;
- регионарный — фактически это метастазы в не удаленных при первой операции подмышечных лимфатических узлах или продолженный рост не распознанного ранее ракового поражения подключичного и надключичного лимфоколлектора;
- местно-регионарный включает сочетание обеих описанных состояний;
- тотальный рецидив предполагает существование метастатической стадии и локального рецидива молочной железы, как правило, подобное распространение относят к генерализации метастазов, поэтому в русскоязычной онкологии этот термин почти не используется.
Частота развития
Вне зависимости от распространенности рака в молочной железе на момент начала терапии и биологических характеристик злокачественной клетки у каждой десятой пациентки в ближайшее десятилетие после удаления грудной железы может развиться местно-регионарный рецидивный процесс.
При раннем раке местная рецидивная опухоль отмечается не чаще 5%, что не исключает появление новообразования в рубце во второй пятилетке после лечения рака молочной железы, некоторые исследования в отдаленный период наблюдения констатировали локальные проявления у каждой 20-й пациентки. При раке молочной железы 2-3 стадии вероятность раннего рецидивирования в рубце превышает 20%.
Изначальное метастатическое поражение лимфоузлов предполагает возврат заболевания у 7 из десяти женщин, при отсутствии опухоли в лимфатическом коллекторе возврат рака возможен только у каждой третьей, но в подавляющем большинстве под «возвратом» понимается именно метастазирование рака молочной железы.
Факторы риска
Вероятность рецидивирования в зоне первичной операции по поводу рака молочной железы зависит:
- от размера опухоли молочной железы, так образования до 2 сантиметров считаются не столь опасными, с другой стороны, внутрипротоковый рак ин ситу — это стадия 0 обладает мощным потенциалом к инициации рецидивных образований — и это случается в каждом шестом случае, что объясняется миграцией злокачественных клеток по молочным протокам железы;
- от массивности поражения подмышечного лимфоколлектора, так при отсутствии метастазов в лимфоузлах подмышечной области вероятность рецидивирования не более 4%, при трёх метастатических лимфоузлах — у каждой десятой, при девяти — уже у каждой пятой, а при 10 — у каждой четвертой может возникнуть рецидивное новообразование;
- от агрессивности рака молочной железы, так высоко злокачественные карциномы, особенно без рецепторов половых гормонов на мембранах клеток, обладающие геном HER2,
- существенно повышается риск возврата злокачественного процесса в месте оперативного лечения при распространении клеток рака по мелким лимфатическим сосудикам и около нервов за пределами опухолевого узла — при сосудистой и периневральной инвазии;
- от объёма первичного лечения, так резекция чревата рецидивом в большем проценте случаев, нежели мастэктомия, поэтому иссечение части груди всегда должно дополняться облучением;
- отказ от применения профилактической или адъювантной химиотерапии, существенно снижающей вероятность рецидивов и метастазов рака молочной железы, тоже откликается негативным прогнозом.

Категории риска
При лечении рака молочной железы официально не принято выделять категории риска, как при раке предстательной железы, поскольку последняя имеет не столь обширное морфологическое типирование. Рак молочной железы представлен огромным разнообразием клеточных видов, все их учесть невозможно, и регулярно список критериев пересматривается и дополняется. Тем не менее, некоторые клиники используют «категории риска» для объяснения пациенткам отдаленных перспектив.
В специальной литературе и клинической практике выделяют критерии неблагоприятного прогноза, обещающие высокую вероятность возврата заболевания в любом виде — метастазирование или рецидивирования.
Не выявлено закономерностей сочетания и численности неблагоприятных признаков, считается, что чем больше критериев найдено при микроскопии и специфических анализах, тем хуже прогноз:
- размер первичного рака в железе более 5 сантиметров,
- опухолевое поражение больше четырех лимфоузлов в подмышке,
- низкодифференцированная структура,
- обладание клетками HER2-геном,
- высокий потенциал деления раковых клеток, обозначаемый как Ki67,
- распространение клеток за пределы узлового образования, что в гистологии указывается как периневральная и лимфоваскулярная инвазии.
Не вписывается в прогностическую программу определяемый только микроскопией и часто такого же объема внутрипротоковый рак молочной железы или DCIS, всегда классифицируемый как in situ или 0 стадия рака при любом размере узла. Злокачественные клетки в DCIS не прорывают базальную мембрану эпителия, то есть внедрения — инвазии нет, но раковые комплексы способны выживать на приличном удалении от материнского узла, что откликается высокой частотой локальных рецидивов и потому требует объемного хирургического вмешательства.
Группа низкого риска
Вероятность появления рецидивной опухоли на грудной стенке и в регионарном лимфатическом коллекторе зависит от индивидуальных особенностей, определяемых при гистологическом исследовании как факторы негативного прогноза рака, и полноты послеоперационного лечения.
Не напрасно пациенток не выписывают из стационара до получения данных послеоперационного морфологического исследования удаленной молочной железы, только на основании гистологии можно назначить адекватное лечение и снизить риск возврата злокачественного процесса.
Изначально низкий риск обещают: небольшой рак молочной железы, «чистые» лимфоузлы, высокая дифференцировка и наличие гормональных рецепторов. Но никто не даст гарантии, что низкая вероятность навсегда избавит от болезни, так же как неблагоприятный прогноз совсем не обязательно приведет к метастазированию — все настолько индивидуально, что в отличие от других специалистов, онкологи никогда не предсказывают течение рака у женщины.
Скорректировать степень риска в сторону снижения помогают дополнение операции лучевой терапией и профилактической химиотерапией или гормональными препаратами при высоком рецепторном статусе.
Не гадайте, что вас ожидает, а регулярно проходите обследование, наши специалисты не пропустят симптомов болезни.
Симптомы
Как и при первичном раке молочной железы первый клинический признак рецидивирования — появление уплотнения в зоне операции. Это может быть плотный узелок под кожей грудной стенки или в оставшейся ткани молочной железы, или в послеоперационном рубце. Как правило, подавляющее большинство женщин находят новообразование в ранней стадии развития — до сантиметра в диаметре и даже меньше.
Как избежать рецидива
Многочисленные исследования доказали равноценное влияние на продолжительность жизни мастэктомии и частичной резекции молочной железы. Тем не менее, сохраняющая репродуктивный орган операция чревата повышением частоты локального рецидива минимально — у каждой десятой, максимально — у каждой третьей. Добавление лучевой терапии на зону резекции и лимфатические регионарные зоны уменьшает процент рецидивов как минимум втрое. Поэтому стандарт лечения включает органосохраняющую резекцию с облучением, которое необходимо начать не позже 12 недель.
Дополнительное локализованное облучение зоны операции «бустом», увеличивающее стандартную дозу до максимальной, вполовину снижает вероятность рецидива. Крайне важна точность послеоперационного облучения, специальные метки, оставляемые хирургом при операции, помогают попасть «лучам» точно в цель.
При невозможности выполнения резекции молочной железы выполняется полное удаление груди — мастэктомия. Реконструктивная мастэктомия с закрытием обширного дефекта тканей грудной стенки собственными тканями — кожно-мышечным лоскутом при большом раковом узле с врастанием в грудную мышцу, дополнительно снижает частоту рецидива на 90%. Разумеется, мастэктомия всегда сочетается с удалением клетчатки со всеми окружающими лимфоузлами — от подмышечных — до подлопаточных.
При мастэктомии лучевая терапия показана уже при трёх метастазах в лимфатических узлах, при меньшем их числе — необходимость определяется размерами ракового узла.
При неблагоприятных факторах прогноза или обнаружении раковых комплексов по линии разреза во время плановой гистологии — проводится химиотерапия.
При гормональной зависимости карциномы пятилетний прием антиэстрогенов каждую вторую женщину избавляет от возможного рецидива.

Диагностика
После мастэктомии обнаружить рецидив несложно, УЗИ мягких тканей грудной стенки помогает определиться с границами новообразования и выполнить прицельную пункцию. Преимущество за тонкоигольной биопсией, позволяющей взять столбик раковой ткани для морфологического и ИГХ-анализа на гормональный состав рецепторов.
При рецидиве в остаточной ткани молочной железы выполняется маммография, но лучевой фиброз затрудняет трактовку снимков. Ясность вносит УЗИ и, разумеется, биопсия. Биопсия обязательна, поскольку постлучевые изменения тканей по плотности могут имитировать рецидивную опухоль.
Лечение
Терапевтический подход к локальному рецидиву аналогичен лечению первичного рака, то есть на первом этапе предпочтительно хирургическое вмешательство. Объем удаления определяется локализацией и размером новообразования, что не исключает повторной органосохраняющей операции. При небольшой железе или выраженных постлучевых изменениях тканей показана мастэктомия.
Если ранее пациентке не проводили облучения послеоперационного поля, после повторного вмешательства стоит провести лучевую терапию. Повторное облучение одного и того же места чревато тяжелыми повреждениями тканей, поэтому не проводится, но возможны исключения, учитывающие исходное состояние тканей.
При регионарном рецидиве в виде метастазов в лимфоузлах над или под ключицей целесообразна цикловая химиотерапия с последующим облучением.
При неоперабельном процессе, в том числе, локализованном рецидиве в сочетании с отдаленными метастазами основное лечение — химиотерапия.
Прогноз
При рецидивной опухоли прогноз не отличается от такового при первичном раке молочной железы, то есть при опухоли до 2 см аналогичен 1 стадии рака и пятилетней выживаемости до 90%. Неоперабельный процесс не сулит долгой жизни, но химиотерапия и гормонотерапия помогают продлить жизнь на годы.
Регулярное наблюдение и своевременное обследование помогают вовремя поставить диагноз и начать лечение. Все знают, что раннее обнаружение — залог успешной терапии, но не менее важен профессионализм наблюдающего специалиста и его клинический опыт. В нашей клинике есть и третье составляющее успеха — отличное и современное оборудование.
Запись на консультацию круглосуточно
Список литературы
- Семиглазов В.Ф. / Роль лучевой терапии в лечении ранних стадий рака молочной железы//Материалы III Российской онкологической конференции
- Coates A.S., Winer E.P., Goldhirsch A et al. /Tailoring therapies—improving the management of early breast cancer: St Gallen International Expert Consensus on the Primary Therapy of Early Breast Cancer 2015// Annals of Oncology 26, 2015.
- Goodwin A., Parker S., Ghersi D., Wilcken N. /Post-operative radiotherapy for ductal carcinoma in situ of the breast-a systematic review of the randomised trials// Breast. 2009 Jun; 18(3).
- Katz A., Strom E., Bucholz T. et.al./Locoregional Reccurence Patterns After Mastectomy and Doxorubicin-based Chemotherapy: Implications for Postoperative Irradiation//J. Clin. Oncol. 2000; 18.
- Litière S., Werutsky G., Fentiman I.S., et.al./ Breast conserving therapy versus mastectomy for stage I-II breast cancer: 20 year follow-up of the EORTC 10801 phase 3 randomised trial// Lancet Oncol. 2012 Apr;13(4).
- Newman L.A. /Management of patients with locally advanced breast cancer// Curr. Oncol. Rep. 2004 Jan;6(1).
что такое, группы риска, симптомы и лечение
Рецидив рака молочной железы нередко развивается даже после прохождения полного курса лечебной терапии. При этом не всегда болезнь снова возобновляет свое течение через год после комплексной терапии – иногда симптомы рецидива рака молочной железы можно заметить через 10-20 лет после проведения лечения. При таком состоянии опухоль способна снова появиться на том же самом месте, или же образоваться в другой груди.
Что делать при повторном возникновении болезни? В таком случае требуется немедленно начинать лечение онкозаболевания, чтобы остановить рост злокачественного новообразования и сохранить здоровье молочных желез.
Что представляет собой рецидив рака груди?

Рецидив рака после мастэктомии, медикаментозного, лучевого или другого вида терапии является опухолью злокачественного течения. Рецидив и метастазы рака груди могут поразить ту же молочную железу, вблизи расположенные лимфатические узлы или же отдаленные ткани железы.
Если рак рецидивировал в другую грудь, онколог рассматривает такое заболевание, как отдельную опухоль, и составляет новый план лечебной терапии. Однако ее метастазирование на костную ткань так же рассматривается как РМЖ и не является отдельной патологией.
Таким образом, различают 3 варианта развития рака:
- Местный – рост числа злокачественных клеток вновь зафиксирован в ранее пролеченной МЖ (в первоначальном месте) либо на послеоперационном рубце. Часто протекает без явных симптомов и расценивается как недостаточность проведенной лечебной терапии.
- Регионарный – количество раковых клеток увеличивается, поражая ткани железы и лимфатических узлов, расположенных в области подмышечных впадин, шеи и зоны декольте (наблюдается в 40% случаев). Патология принимает более агрессивную форму.
- Метастатический (отдаленный) – раковые клетки разносятся по кровеносной и лимфатической системе, заражая отдаленные участки организма, например, печень, мозг, легкие. Так же очаг РМЖ может зародиться в противоположной груди.
Если опухоли удалось рецидивировать, она будет развиваться более быстро и агрессивно, что, разумеется, отрицательным образом скажется на здоровье женщины.
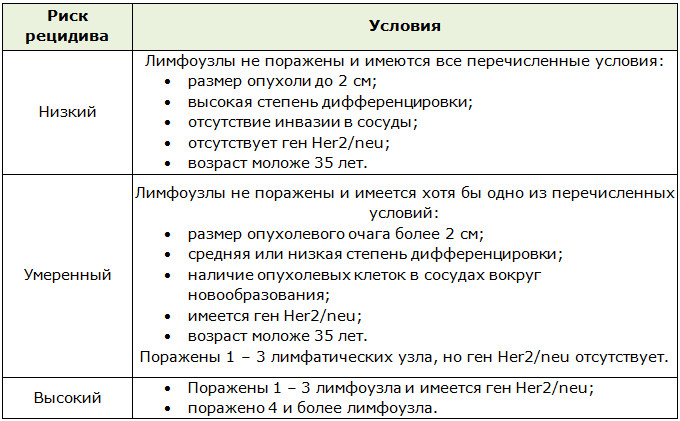
Когда новообразованию удается повторно рецидивировать?
Риск рецидива | Факторы |
| Низкий | РМЖ не затронул близрасположенные лимфатические узлы и сосуды, и размер опухоли сравнительно небольшой – до 2 см. Возраст пациентки – до 35 лет. Предпринято несколько вариантов лечебной терапии. |
| Умеренный | Зона поражения превышает 2 см., и патология распространяется на рядом расположенные кровеносные сосуды. Выявлен ген Her2/neu либо поражены 1-3 лимфоузла. |
| Высокий | РМЖ был обнаружен на последних стадиях. Поражены 1-4 и более лимфатических узлов и сосудистая сетка рядом с опухолью, выявлен ген Her2/neu, возраст пациентки – старше 35-40 лет. Болезнь агрессивна и дала метастазы, повышена скорость деления злокачественных клеток. Предпринят 1 вариант лечебной терапии. |
Если больная своевременно обратится к доктору, что позволит вовремя приступить к комплексной терапии болезни, выживаемость в таком случае составляет 60%.
В каких случаях онкология развивается повторно
Когда опухоль в груди развивается повторно, это еще сильнее пугает больную, нежели предыдущее заболевание. Женщина начинает думать, что болезнь невозможно излечить полностью, и, несмотря на предпринятые меры, она будет возникать постоянно.
В основном, проявление новообразования происходит в том случае, когда во время лечения РМЖ врачам не удается полностью уничтожить раковые клетки, особенно если они успели проникнуть в здоровые ткани груди или разнестись вместе с кровью в иной орган. При проведении операции оценить степень распространения злокачественных клеток трудно, так как без их активного роста выявить новое расположение опухоли невозможно.
По мнению онкологов, если после проведения основной терапии прошло более 6 месяцев, и при сдаче анализов не было выявлено никаких метастазов, то повторное обострение болезни считается рецидивом. Если же в послеоперационный период были выявлены новые опухолевые клетки, значит, патология была не полностью излечена.
Также рецидивом можно назвать появление злокачественного новообразования в другом органе. В таком случае опухолевые клетки перенеслись по организму вместе с током крови, что и вызвало новый очаг заражения. Данное явление врачи называют метастазированием первичного новообразования.
Появление метастаз в организме женщины гласит, что некоторые злокачественные клетки во время терапии были к ней нечувствительны. Такой показатель требует срочной повторной операции или консервативной терапии, которая позволит сохранить здоровье пораженного органа.
Факторы развития патологии

Рецидив рака груди у женщин часто появляется в результате конкретных обстоятельств. Сегодня онкологам известен ряд факторов, которые служат началом повторного возникновения болезни:
- Форма рака – если патология протекает в агрессивной форме, риск рецидива опухоли вырастает в несколько раз.
- Стадия, при течении которой врачам удалось выявить заболевание – если его обнаружили поздно, процент появления рецидива велик.
- Большое количество раковых клеток в женском организме.
- Поражение лимфоузлов и кровеносных сосудов, расположенных вблизи молочных желез.
- Скорость роста опухоли и ее размер.
- Рождение первого ребенка после 30-35 лет.
- Ранняя менструация и поздний климакс.
- Определенный тип онкогенов, находящихся в раковых клетках, что также часто вызывает развитие болезни.
После завершения лечения доктор оценит риск появления рецидива онкологического процесса, а также проинформирует женщину о необходимости ежегодного прохождения обследования груди.
Как правило, симптомы рецидива заболевания можно заметить в любое время после проведения терапии, однако зачастую болезнь начинает снова развиваться через 3-5 лет по окончании лечебного курса.
Кто находится в группе риска
Чтобы избежать рака груди, требуется узнать, какие группы женщин наиболее подвержены развитию патологии.
Как показывает статистика, чаще всего болезнь диагностируют у женщин 35-45 лет, однако иногда заболевание встречается у более молодых представительниц прекрасного пола, достигших возраста 25 лет.
Для начала, в группу риска можно отнести тех женщин, у которых присутствует наследственная предрасположенность к заболеванию. Если по женской линии наблюдались раковые опухоли груди, болезнь развивается в 50% случаев.
Обычно это зависит от вида предыдущей терапии (имеется в виду, что предпринят только один вариант лечения, а не их сочетание):
Тип лечения | Риск повторения РМЖ |
| После лучевой терапии | Рак развивается в 5-10% случаев |
| После проведения радиолечения | Риск повторно наблюдать заболевание присутствует у 20-40% пациенток |
| После мастэктомии | Наблюдать рецидив злокачественной опухоли приходится в 60% случаев |
Благодаря научным исследованиям удалось выяснить, что женщин, у которых в крови присутствуют гены рака, тоже стоит включить в группу риска. Выглядят такие гены следующим образом: BRCA-II в хромосоме 13 и BRCA-I в хромосоме 17. В таком случае метастазирование может повысить риск развития болезни еще на 10%.
Какую опасность несет повторный РМЖ

Если новообразования молочных желез не излечить вовремя, болезнь будет стремительно прогрессировать. У 10% пациенток, обратившихся к врачу, заболевание уже сопровождается метастазами. Сложность лечения заключается в том, что таких больных нельзя подвергать проведению операции, поскольку у них наблюдается активное прорастания метастазов или же выявлено общее истощение организма.
Главная опасность заболевания заключается в высокой смертности женщин, которым не помогло лечение или же врачи не успели провести операцию. Вероятность полного излечения болезни составляет всего 30%, в то время как в остальных случаях возможен рецидив заболевания.
Как происходит распространение клеток, которые не были уничтожены во время лечения? Вместе с лимфатической жидкостью или током крови злокачественные клетки способны проникать во многие органы. К ним относится:
- Легкие.
- Брюшина.
- Мозг.
- Скелет.
- Печень.
- Грудная клетка.
- Здоровые ткани груди и пр.
В таком случае терапия проводится более комплексно, что позволит полностью уничтожить раковые клетки.
Рак – опасная патология, быстро развивающаяся в организме, поэтому раннее выявление симптоматики поможет предотвратить развитие большой опухоли, способной привести пациентку к летальному исходу.
Первые симптомы возвращения болезни

Рецидив раковой опухоли можно выявить самостоятельно – для этого достаточно аккуратно прощупывать грудь и ежегодно посещать врача. Если заболевание полностью излечилось, молочная железа будет мягкой и без твердых бугорков и уплотнений.
На развитие рецидива обычно указывают следующие признаки:
- Изменение цвета и вида сосков.
- Патологические выделения из соска.
- Жжение в груди.
- Зуд на коже молочной железы, наличие язв, трещин.
- Отдельный воспаленный участок груди стал мраморно-подобного цвета.
- Температура тела стала выше.
- Появление красного пятна на пораженном участке груди.
- Изменение размера и контура пораженной железы.
- Общее истощение организма.
- Снижение аппетита.
- Потеря веса.
- Анемия и гипертермия.
- Быстрая утомляемость, вялость, упадок сил.
Как правило, именно такие симптомы указывают на повторное метастазирование, лечение которого требуется проводить в короткие сроки. Во избежание рецидива после терапии опухоли следует регулярно посещать врача (особенно первые пару лет), чтобы удалось вовремя обнаружить заболевание.
Необходимые диагностические меры

Чтобы выявить прогноз заболевания, женщине следует пройти все диагностические мероприятия, которые позволят поставить точный диагноз, а также выявить структуру и степень злокачественного новообразования.
Врач сможет выявить РМЖ при помощи осмотра больной и выслушивания симптомов, которые ее тревожат. Также для подтверждения диагноза понадобится пройти маммографию.
Если при помощи таких диагностических методов не удастся подтвердить заболевание, больной понадобится пройти такие методы исследования:
- Рентгенография.
- Компьютерная томография.
- Радиоизотопное сканирование.
- Анализы крови (общий и на онкомаркеры).
- УЗИ.
- МРТ.
- ПЭТ.
Если женщине ранее проводилось хирургическое лечение, понадобится осмотр рубцов, так как именно в них чаще всего развивается повторная опухоль.
Проведение биопсии необходимо для того, чтобы различить образование новой обособленной опухоли или рецидивирование старой. При анализе биопсии получится выявить чувствительность раковых клеток к таргетному и гормональному лечению.
К какому врачу обратиться
В послеоперационный период и в качестве профилактики рака груди требуется посещать маммолога. Если же он выявит у женщины онкологию, врач направит больную непосредственно к онкологу, так как только узкий специалист поможет провести комплексное лечение.
Если болезнь метастазировала на другие органы, например, в матку и яичники, то женщину также будет наблюдать специалист соответствующей области — гинеколог.
Методы лечебной терапии после повторения РМЖ
Радикальное лечение заболевания проводится несколькими методами. К ним относится:
- Местное лечение болезни, подразумевающее проведение операции, брахитерапии или лучевой терапии.
- Системное лечение, при котором больной назначают таргентные или гормональные лекарства, а также проведение химиотерапии.
Как правило, чаще больной выписывают местное лечение при тяжелом течении болезни. Если же рак развивается на начальном этапе, понадобится проведение системной терапии. Также вид лечения зависит от частоты рецидивов, ведь иногда они могут встречаться часто – это зависит от неполного уничтожения раковых клеток, которые со временем образуют новую опухоль.
Если болезнь выявлена у женщины впервые, помочь побороть ее могут лекарственные средства. Однако польза от такой терапии будет лишь в том случае, если пациентка будет строго соблюдать инструкцию по применению препаратов, не нарушать дозировку, а также следовать советам врача.
Нередко повторное появление болезни указывает на агрессивность раковых клеток, которые не так-то просто уничтожить. В таком случае больной назначается комплексная терапия (и местная, и системная), что позволит полностью побороть все патологические клетки, которые могли попасть в органы, ткани или лимфатические узлы пациентки во время первого лечения.
Повторная терапия несет больше шансов на полное выздоровление, ведь доктор проводит тщательное обследование, чтобы понять, куда именно распространились раковые клетки в женском организме. Но если больная несвоевременно посетит доктора, рак молочных желез может поразить большую часть груди – в результате этого требуется ее удаление (частичное, полное, с иссечением части лимфоузлов).
Как обезопасить себя от рецидивов и метастазов?

Что можно сделать, чтобы избежать повторного развития болезни? Для предотвращения рецидива необходимо обязательно проводить профилактику, которая позволит избежать возобновления патологии.
Как правило, профилактические мероприятия требуется проводить сразу после терапии, так как онкологические клетки способны попадать в русло крови, тем самым вызывая повторное заболевание.
В профилактические мероприятия входит:
- Прием специальных лекарств, которые уменьшают выработку эстрогена (гормон) – это не позволяет раковым клеткам расти, образуя в груди или другом органе новую злокачественную опухоль.
- Контроль веса – нельзя резко худеть и набирать массу. Показатель веса должен соответствовать вашему росту и возрасту.
- Отказ от алкоголя и курения, переход на сбалансированное питание.
- Наблюдение у маммолога каждый 6 месяцев.
- Проведение лечебной гимнастики и массажа, особенно после оперативного вмешательства.
- Регулярное самообследование МЖ.
- Не допускать обострения хронических патологий.
- Прием любых гормональных средств, в том числе и контрацептивов, необходимо согласовывать с лечащим врачом.
- Молодые женщины могут планировать беременность с последующим ГВ.
- Прием витаминных комплексов и препаратов, стимулирующих работу иммунной системы.
Сколько обычно требуется пить лекарства? Чтобы избежать повторного заражения, следует принимать препараты на протяжении полугода.
Прогнозирование болезни
При рецидиве местного типа после проведения мастэктомии, во время которой лимфатические узлы не были поражены, выживаемость больных составляет 75%. В таком случае излеченные пациентки смогут прожить более 5 лет. Если в груди были обнаружены метастазы, срок жизни женщин составляет 3 года. Выявление заболевания на ранней стадии позволяет полностью излечить болезнь.
После терапевтического лечения пациентке требуется проводить профилактику, а также следить за состоянием груди – если на ней появятся наросты, жжение, уплотнения, шелушения, требуется обязательно посетить доктора, так как такие признаки свидетельствуют о развитии злокачественной опухоли. В таком случае только врач сможет дать правильную оценку данного состояния. Также он осмотрит рубец, чтобы понять, какое именно заболевание развивается у больной, и даст направление на анализы.
Своевременное обнаружение болезни поможет полностью ее излечить, что сохранит жизнь больной и не сделает ее сложной.
 Загрузка…
Загрузка…вероятность, лечение, прогнозы и отзывы
Содержание статьи:
После завершения адъювантной терапии пациентка чувствует облегчение и иногда страх. Боязнь, что наступит рецидив рака груди, не дает покоя более 50% женщин. Специалисты всего мира утверждают, что такой риск есть. Но онкология возвращается при условии ряда провоцирующих факторов. Болезнь имеет код по МКБ-10 – С50.
Виды и признаки рецидива

Рецидив рака называют поздним, если он наступает через 2-4 года успешного лечения
Медики выделяют два типа повторной онкологии молочной железы:
- Ранний. Опухоль возникает примерно через 2-4 месяца после окончания основной терапии.
- Поздний. Рак рецидивирует через 2-4 года после успешного лечения.
Симптомы онкологии такие же, как и при первичном образовании. Общее ухудшение самочувствия пациентки, выделения из соска, трещины на нем, образование темных корочек в зоне локации опухоли (не всегда). Признаки рецидива после мастэктомии — это ощущение бугорка, уплотнения в прооперированной молочной железе. Болезненность груди в определенные периоды цикла. Ощущение тяжести в ней.
Вероятность рецидива
Риск развития повторной онкологии после успешного лечения зависит от типа выявленного у пациентки образования и особенностей проведенной терапии. Хуже всего, если обнаружена 3 или 4 степень онкологии. Причем рецидив может развиваться локально, в том же месте, где была предыдущая опухоль, или метастазировать — перемещаться, разрастаться в иные ткани.
Категории риска для рецидива рака молочной железы
Есть вероятность рецидива рака молочной железы в послеоперационном рубце, в подмышечных или подключичных подкожных лимфатических узлах. При этом риск развития повторной онкологии может сохраняться для пациентки на протяжении всей жизни, но оставаться минимальным. Либо рецидив возникает очень быстро. Все зависит от типа удаленной или пролеченной опухоли.
Прогноз

Вероятность рецидива зависит от величины раковых клеток проникших в лимфоузлы
После удаления образования врач-патолог тщательно изучает его. На определение дальнейшего прогноза влияют такие факторы:
- Вероятное проникновение раковых клеток в лимфатические узлы (метастазирование). Чем их больше, тем выше риск развития повторной проблемы. Согласно отзывам и статистике, рецидив РМЖ в лимфоузлах возникает примерно в 20% случаев при условии выявления онкологии на поздних стадиях.
- Активность HER2.
- Размер опухоли. Чем он больше, тем выше возможные риски для пациентки.
- Наличие мест крепления эстрогенов и прогестеронов (гормональных рецепторов) в злокачественных клетках.
- Скорость деления патологических клеток.
При выявлении ряда провоцирующих факторов назначается дополнительное лечение прицельного действия. Выживаемость при рецидиве рака молочной железы составляет около 65%.
Дополнительные причины развития рецидива
Прогноз относительно рецидива РМЖ строится по ряду дополнительных провоцирующих факторов.
Возраст

Чаще рецидивы встречаются у пациенток до 35 лет. Обусловлено это тем, что в молодом организме опухолевый процесс ведет себя более агрессивно. Деление клеток происходит быстрее, что значительно ухудшает прогноз для пациентки. Молодые женщины с первичным РМЖ должны получить консультацию онколога относительно генетического контроля.
Вес
Лишние килограммы (а точнее ожирение) повышают риск развития повторной онкологии. Тестостерон и андростендион, имеющиеся в большом количестве у тучных людей, в жировой ткани превращаются в эстрон, который способствует дальнейшему развитию патологического процесса.
Употребление алкоголя

Вероятность развития рака и его рецидива напрямую зависит от количества употребляемого спиртного
Спиртные напитки провоцируют повышение уровня эндогенного эстрогена в крови пациентки. Он в свою очередь является причиной развития первичной опухоли и рецидива РМЖ, поскольку негативно действует на ткани молочных желез. Каждые регулярно употребляемые 10 мл алкоголя – риск снова столкнуться с онкологией.
Расовая принадлежность
Считается, что у представительниц негроидной расы первичная и повторная онкология случаются чаще, чем у женщин европеоидной группы. Обусловлено это тем, что женщины из группы риска имеют менее полный доступ к качественному медицинскому обслуживанию. Соответственно болезнь чаще выявляют на поздних стадиях, что является неблагоприятным прогностическим фактором.
Для полноценного прогноза рецидива рака молочной железы после мастэктомии желательно поддерживать постоянную связь с лечащим онкологом. Особенно на первых порах после удаления опухоли.
Диагностика рецидива РМЖ
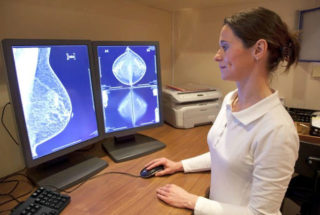
Повторное маммографическое обследование проводят при локализованном рецидиве
Диагностика повторного рака зависит от того, где он проявился. Если это локализованная онкология, её устанавливают такими методами:
- маммография;
- УЗИ молочной железы;
- КТ или МРТ грудной клетки.
Если рак метастазировал, показаны такие методы диагностики:
- КТ всего тела, поскольку метастазы могут поражать любую его часть и полость;
- радиоизотопное исследование костных тканей;
- обследование ПЭТ-КТ с FDG, что позволяет получить более точное представление о выявленных очагах метастазов.
В обязательном порядке пациентке назначают биохимический анализ крови и биопсию локального образования. Из местастазов также берут образцы биоматериала для определения her 2-статуса. На основании результатов подбирается тактика лечения.
Чаще РМЖ метастазирует в печень, легкие, кость, кожу, лимфоузлы.
Методы лечения
Противоопухолевый препарат
Терапия рецидива рака молочной железы полностью зависит от его типа. Если онкология обнаружена локально (в шве, рубце, тканях молочной железы), проводится оперативное вмешательство. Затем проводится дополнительное адъювантное лечение. Могут назначаться противоопухолевые препараты, такие как Герцептин и ему подобные.
Метастазирующую онкологию лечат лекарственными препаратами. Для усиления терапевтического эффекта используют лучевую, гормональную или химиотерапию. Врачи уверяют, что от метасиазирующей онкологии полностью избавиться невозможно. Но при должном лечении и постоянном наблюдении пациентка будет жить привычной жизнью еще долго.
После химиотерапии пациентка может выглядеть не очень хорошо (похудение, отсутствие волос на теле). Но позже все восстанавливается.
Профилактика рецидива РМЖ

Для максимальной защиты организма от рецидива онкологического заболевания необходимо отказаться от никотина
Чтобы максимально защитить организм от развития онкологии, врачи рекомендуют придерживаться таких правил:
- вести здоровый образ жизни;
- отказаться от алкоголя и никотина;
- не подставлять грудь прямым лучам солнца;
- регулярные занятия спортом увеличивают шанс на здоровую жизнь;
- избегать стрессовых ситуаций и травм молочной железы;
- полноценно и правильно питаться с обилием овощей, фруктов в рационе.
Чтобы вовремя определить возможное развитие рецидива, врачи рекомендуют делать следующее:
- Регулярно самообследовать грудь. Сразу после операции она будет болезненной или утратившей чувствительность. Но со временем все становится на свои места и женщина способна понять, что именно вызывает её беспокойство в молочной железе.
- Обо всех обнаруженных изменениях, увеличениях сообщать лечащему онкологу, даже если на первый взгляд они кажутся незначительными.
- Обращать внимание на резко изменившееся в худшую сторону самочувствие. Особенно если оно задерживается на несколько дней и более, увеличивается в интенсивности.
- Ежегодно делать маммограмму, посещать лечащего онколога, поскольку рецидив может проявляться постепенно.
Внимание к себе первостепенно. Поэтому заботьтесь о своем здоровье максимально полно.
Психологический фактор

Повторная терапия против рака переносится увереннее
Ранее больные пациентки, перенесшие рак молочной железы, часто склонны к постоянному ощущению страха перед новой бедой. Специалисты рекомендуют не жить с этим. Если мучают опасения, стресс лучше сбрасывать и снижать неприятные эмоции в общении с подругой, врачом или психотерапевтом. Важно не умалчивать о своих мыслях, делиться ими в полной мере. Опытный психолог или психотерапевт поможет максимально справиться с эмоциями и вернуться к полноценной жизни.
Согласно отзывам о лечении рецидива РМЖ пациентки переносят повторную терапию более уверенно. Справляются с болезнью назло онкологии. Важно лишь верить в себя и любить жизнь.
Алина. У меня соседка лечила РМЖ. Прошла операцию, химию, лучевую. Все было относительно хорошо около двух лет. Потом что-то нашли снова. Сейчас опять лечится, чтобы больше не болеть. Врачи говорят, что прогнозы хорошие. Да и сама соседка не унывает. Как-то по-новому полюбила жизнь что ли, начала все с чистого листа.
Яна. У моей бабушки был рецидив РМЖ в 55 лет после 6 лет от последнего лечения. Метастазы. Лечили гормонально и облучали. Бабуля умерла в возрасте 69 лет вполне в здравом уме, и жизнерадостной. Можно сказать, что прожила свою долгую полноценную жизнь. С местными врачами она даже дружила.
почему нельзя делать операцию при метастазах? Операции на метастазы при онкологии
Какие операции проводят при метастазах? Насколько эффективно хирургическое лечение при запущенном раке? Каковы прогнозы? Паллиативная хирургия. Вмешательства при метастатическом раке в печени, легких, головном мозге, брюшине. Где можно пройти лечение в Москве?
Любая злокачественная опухоль в первую очередь опасна своей способностью к метастазированию. Раковые клетки могут проникать в кровеносные сосуды и распространяться в разные части тела, давая начало новым очагам. Если у пациента обнаруживают отдаленные метастазы и диагностируют рак IV стадии, прогноз обычно неблагоприятный. Но это вовсе не означает, что больному уже ничем нельзя помочь.
Иногда при метастатическом раке удается провести местное лечение. Если метастаз один, либо их немного, и они имеют небольшие размеры, их можно удалить хирургическим путем. В случаях, когда радикальное лечение невозможно, паллиативные методы, в том числе паллиативная хирургия, помогают продлить жизнь, улучшить её качество, избавить от боли и других симптомов.
Операции при метастазах в печени
Если в печени обнаружены одиночные метастазы, можно провести хирургическое лечение: лобэктомию (удаление доли), сегментэктомию (удаление сегмента), атипичную резекцию (краевую, плоскостную, поперечную, клиновидную).
Иногда при одиночных метастазах (один очаг не более 0,7 см или 2–4 очага не более 0,3 мм), которые не прорастают в кровеносные сосуды, можно выполнить трансплантацию печени.
Если резекция и трансплантация невозможны, прибегают к методам интервенционной хирургии:
- Радиочастотная аблация — процедура, во время которой хирург вводит в опухолевый узел электрод и подает на него ток высокой частоты. Это приводит к сильному нагреванию и разрушению ткани.
- Эмболизация — введение в сосуды опухоли эмболизирующего препарата, который нарушает приток крови к опухолевым клеткам. Еще более эффективно работает химиоэмболизация, когда эмболизирующий препарат вводят в сочетании с химиопрепаратом.
Если метастазы в печени приводят к нарушению оттока желчи и механической желтухе, проводится наружное или наружно-внутреннее дренирование. Врачи Европейской онкологической клиники выполняют стентирование желчевыводящих путей. В месте сужения устанавливают стент — металлический полый каркас с сетчатой стенкой.

Операции при метастазах в легких
Как и печень, легкие — один из излюбленных органов для метастазирования многих видов рака. Показания к операциям при метастазах в легких в последнее время расширились. Тем не менее, к хирургическому лечению прибегают очень редко, основным методом остается химиотерапия.
Операцию можно проводить только при определенных условиях:
- Узел в легком единичный, либо их не более трех.
- Первичная опухоль удалена, нет рецидива.
- В течение 6 месяцев не возникают новые метастазы.
- У пациента нет других серьезных проблем со здоровьем, общее состояние позволяет перенести сложное хирургическое вмешательство.
Операции при метастазах в брюшине
Брюшина — тонкая пленка из соединительной ткани, которая выстилает изнутри стенки брюшной полости, покрывает внутренние органы. Если в ней возникают очаги ракового роста, такое состояние называется канцероматозом брюшины. При этом развивается асцит — скопление жидкости в брюшной полости.
Врачи Европейской онкологической клиники выполняют лапароцентез (прокол брюшной стенки и эвакуацию жидкости под контролем УЗИ), установку перитонеальных катетеров, паллиативные хирургические вмешательства:
- Перитонеовенозное шунтирование — отведение жидкости из брюшной полости в вену при помощи катетера с клапаном.
- Оментогепатофренопексия — операция, во время которой сальник (складку брюшины) подшивают к печени и диафрагме, в результате улучшается отток асцитической жидкости.
- Деперитонизация стенок брюшной полости — иссечение участков брюшины, благодаря чему открываются дополнительные пути для оттока жидкости.
Операции при метастазах в плевре
Плевра — подобно брюшине, тонкая пленка из соединительной ткани. Она выстилает стенки грудной полости и покрывает легкие. При распространении в неё раковых клеток развивается канцероматоз и экссудативный плеврит — скопление жидкости между плевральными листками, которое мешает дыханию.
В Европейской онкологической клинике при экссудативном плеврите, вызванном онкологическим заболеванием, проводят следующие виды хирургического лечения:
- Плевроцентез (прокол в стенке грудной полости и выведение жидкости) с применением современной американской системы Pleurocan.
- Плевродез — процедура, во время которой листки плевры склеивают, в итоге между ними перестает накапливаться жидкость.
Операции при метастазах в головной мозг
Если в мозге обнаружено не более четырех очагов размерами до 35 мм, применяют стереотаксическую радиохирургию. На опухоль с разных сторон направляют пучки радиоволн. По отдельности каждый из них слаб, но в точке, где они сходятся, их интенсивность многократно возрастает. Таким образом, раковые клетки разрушаются, а окружающая их здоровая ткань остается неповрежденной.
Операции при метастазах головного мозга наиболее эффективны в сочетании с химиотерапией и лучевой терапией.
Если удалить очаги не получается, проводят паллиативные хирургические вмешательства. Их цель — уменьшить отек головного мозга, остановить кровотечение. Это помогает существенно улучшить состояние пациента.
В Европейской онкологической клинике операции при метастазах рака выполняют опытные хирурги-онкологи в условиях превосходно оснащенной операционной. У нас можно пройти комплексное лечение по современным стандартам при злокачественных опухолях любой стадии.
Запись на консультацию круглосуточно
Рецидивы рака молочной железы после органосохраняющего лечения
Пак Д.Д., Рассказова Е.А.
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
Опубликовано: Журнал «Онкохирургия», 2012, том 4, №2.
Рассмотрены особенности рецидивов рака молочной железы в зависимости от возраста пациенток, гистологического типа опухолевого узла, проведения лучевой терапии, а также от иммуногистохимических данных.
Проведен ретроспективный анализ результатов лечения 435 пациенток, которым с 2000 по 2006 гг. выполнены органосохраняющие операции (радикальные резекции) при раке молочной железы.
Характеристика пациенток по стадиям: 0 – 5 (1,1%), I – 181 (41,3%), IIА – 154 (35,3%), IIБ – 44 (10%), IIIА – 51 (11,6%), IIIВ – 1 (0,2%), IIIС – 2 (0,5%). Лучевая терапия проведена у 296 (67,6%) больных.
По стандартам лечения с учетом показаний проводили курсы полихимиотерапии по схемам CAF, АС, ТАС, АТ. Число курсов полихимиотерапии составило 4-6.
За 5-летний срок наблюдения диагностированы рецидивы у 10 (2,3%) больных, до 10-летнего срока наблюдения – у 20 (4,6%).
Самый высокий процент рецидива выявлен при НЕR2-подтипе РМЖ (10%), на 2 месте – трижды-негативный РМЖ (6,1%), на 3 месте – люминальный А подтип (3,1%).
Лечение рецидивов заключалось в следующем: удаление оставшейся части молочной железы – у 14 пациенток, их которых у 5 удаление молочной железы дополнено интраоперационной ФДТ, у 5 – подкожное удаление молочной железы с одномоментной реконструкцией, что связано с возможностью данного вмешательства. Одной пациентке из-за множественных отдаленных метастазов проведена полихимиотерапия.
Заключение. С учетом новых данных о подтипах РМЖ и результатов нашего исследования можно рекомендовать не выполнять лучевую терапию после органосохраняющих операций при узловых образованиях 1 см и меньше, при благоприятных морфологических критериях (отсутствие мультицентричности, раковых эмболов по периферии узла и в ткани молочной железы, отсутствие инвазивного протокового рака III степени злокачественности, а также трижды-негативного и НЕR2 подтипа РМЖ).
На частоту появления рецидивов влияют стадия РМЖ, молодой возраст пациенток, гистогенез и подтип опухоли. При сочетании неблагоприятных прогностических факторов следует прибегать к реоперации на молочной железе.
Ключевые слова: молочная железа, органосохраняющее лечение, рецидивы рака молочной железы.
Рак молочной железы (РМЖ) занимает 1 место в структуре онкологической заболеваемости в РФ среди женского населения и имеет постоянную тенденцию к росту. В настоящее время в России ежегодно регистрируют более 50 000 новых случаев рака молочной железы (в 2009 г. – 54 315) и более 23 000 смертей (в 2009 г. – 23 517), при этом у 62% заболевших выявляют относительно ранние (I-II) стадии заболевания. Следует отметить, что в России за последние 10 лет удельный вес I-II стадий РМЖ возрос на 10%, увеличилось число больных, выявленных при профилактических осмотрах (с 14,9% до 21,9%).
За последние годы сделано много важных разработок в хирургическом лечении пациенток с РМЖ. При начальных стадиях заболевания возможно выполнение органосохраняющих операций с или без реконструктивно-пластического компонента. Лечение планируют при участии хирурга, химиотерапевта, радиолога и морфолога, что позволяет наилучшим образом сочетать локальные и системные методы терапии.
В последние годы наметились новые подходы к лечению РМЖ, связанные с уменьшением объема оперативного вмешательства на молочной железе и на лимфатических путях без нарушения онкологического радикализма. Среди причин отхода от устоявшейся в течение десятилетий агрессивной хирургической тактики:
- увеличение числа больных с ранними стадиями рака;
- создание эффективной комбинации оперативного вмешательства с лучевым, химиогормональным и таргетным воздействием;
- пересмотр клинико-биологических концепций течения опухолевого процесса;
- совершенствование инструментальной диагностики.
Радикальная резекция молочной железы является органосохраняющей операцией и предусматривает удаление сектора молочной железы вместе с опухолью, части подлежащей фасции большой грудной мышцы, а также подключичной, подмышечной, подлопаточной клетчатки с лимфатическими узлами в едином блоке. При этой операции удаляют не менее 1/4 или 1/3 молочной железы, отступая 3-3,5 см от пальпируемого края опухоли. При локализации опухоли в медиальных отделах молочной железы операция может быть выполнена из двух разрезов кожи – на молочной железе и в подмышечной области. Радикальную резекцию молочной железы выполняют с обязательным интраоперационным морфологическим исследованием соскобов с краев резекции молочной железы.
В мире наиболее часто используемыми вариантами органосохраняющих операций являются лампэктомия (в российском варианте – секторальная резекция с подмышечной лимфаденэктомией) и квадрантэктомия (радикальная резекция).
Рандомизированное исследование результатов двух операций – лампэктомии и квадрантэктомии – было проведено в 1990 г. В исследование были включены больные с максимальным размером опухоли до 2,5 см (всего 705 пациенток). Всем больным проводили послеоперационное облучение. Развитие отдаленных метастазов и выживаемость больных в группах оказались идентичными, но у больных, перенесших лампэктомию, местный рецидив развивался достоверно чаще, чем у оперированных в объеме квадрантэктомии (7,0% и 2,2% соответственно).
С 1973 г. в Национальном институте по лечению рака (Милан) проводилось рандомизированное исследование, в которое включались больные с размером первичной опухоли до 2 см и без пальпируемых подмышечных метастазов. Радикальная мастэктомия по Halsted была выполнена 349 больным (1-я группа), квадрантэктомия с послеоперационным облучением – 352 (2-я группа). Квадрантэктомия предполагала иссечение опухоли и 2-3 см прилежащей здоровой ткани молочной железы с подлежащей фасцией и кожей, а также подмышечную лимфаденэктомию всех трех уровней. Если опухоль локализовалась в верхненаружном квадранте, то ее удаление и лимфаденэктомию выполняли единым блоком. Статистически значимых различий между группами больных по безрецидивной и общей выживаемости не отмечено.
Наконец, минимальная по объему удаляемой ткани молочной железы лампэктомия (lump – глыба, кусок, комок) была разработана в ходе исследований Национального проекта дополнения операций на молочной железе и кишечнике (NSABBP, США). При такой операции выполняли удаление опухоли и лимфаденэктомию из двух отдельных разрезов: через дугообразный кожный разрез, ориентированный по кожным складкам (иссечение кожи и подлежащей фасции было необязательным, запас здоровых тканей железы не регламентировался) удаляли опухоль; через кожный разрез, пересекающий подмышечную область в горизонтальном направлении, проводили лимфаденэктомию. В исследование входили больные (n=1851) с величиной опухоли не более 4 см. Сравнивали группы больных с лампэктомией (1-я группа), лампэктомией с лучевой терапией (2-я группа), модифицированной радикальной мастэктомией (3-я группа). При поражении лимфатических узлов проводили адъювантную химиотерапию. При 12-летнем наблюдении местный рецидив в молочной железе развился у больных 1-й группы в 35% случаев, 2-й группы – в 10%. Достоверные различия общей выживаемости и выживаемости без отдаленных метастазов между сравниваемыми группами отсутствовали. Общий вывод о равной эффективности органосохраняющего лечения и радикальных мастэктомий подтвержден и при 20-летнем наблюдении. Частота местного рецидива после лампэктомии составила 39,2%, после лампэктомии с облучением – 14,3% (p<0,001).
U. Veronesi и соавт. (1995), анализируя результаты лечения 1973 больных со средней продолжительностью наблюдения 82 мес., пришли к выводу, что при размере опухоли до 2,0-2,5 см вполне возможно проведение органосохраняющего лечения. В группе больных, оперированных в объеме радикальной мастэктомии по Холстеду, квадрантэктомии с лучевой терапией, лампэктомии с лучевой терапией и квадрантэктомии без облучения, показатели общей выживаемости не разнятся между собой, однако частота развития местных рецидивов после лампэктомии с облучением и квадрантэктомии без облучения значительно выше, чем после квадрантэктомии с облучением и радикальной мастэктомии.
Сегментарная резекция занимает промежуточное положение между квадрантэктомией и секторальной резекцией. Сегмент молочной железы удаляют до фасции большой грудной мышцы, отступя от краев опухоли не менее 10 мм. Кожа над этим участком железы также иссекается. В ходе этой операции удаляют меньший объем тканей в сравнении с квадрантэктомией и, соответственно, достигают лучшие косметические результаты.
Сегментарная резекция, которая была описана К. Аspergen и соавт. (1988), является операцией выбора в большинстве скандинавских стран и Европе, в то время как лампэктомия широко используется в США, где в соответствии со стандартами NССN проведение послеоперационной лучевой терапии является обязательным.
Большинство рандомизированных исследований убедительно доказывают, что при тщательном отборе больных в группы для проведения органосохраняющего лечения показатели их выживаемости не уступают таковым в группах пациенток, перенесших радикальную мастэктомию (табл. 1).
Таблица 1. Сравнение результатов органосохраняющего лечения с радикальной мастэктомией.
| Авторы | Частота местного рецидива после | Показатели общей выживаемости |
|
|---|---|---|---|
| органосохраняющего лечения | РМЭ | ||
| V.V. Vishnyakova и соавт. | 9,1% (7-летние) | 2,6-3,7% | Одинаковы |
| U. Veronesi и соавт. | 8,8% (20-летние) | 2,3% | Одинаковы |
| B. Fisher и соавт. | 39,2-14,3% (20-летние) | Одинаковы | |
| J.A. Van der Hage и соавт. | 10,8% | 5,9% | Одинаковы |
| С.М. Портной и соавт. | 4,0-5,5% | 2,4% | Одинаковы |
На основании сравнительного анализа рандомизированных и нерандомизированных клинических исследований различных вариантов органосохраняющего лечения рака молочной железы I и IIА стадий можно сделать вывод, что объем оперативного вмешательства не оказывает существенного влияния на результаты 5-летней выживаемости.
В последнем метаанализе EBCTCG, оценивающем вклад лучевой терапии в органосохраняющее лечение РМЖ, сравнивали две грандиозные группы больных: 3673 – органосохраняющая операция с лучевой терапией и 3638 – только органосохраняющая операция. Лучевая терапия снижала не только частоту местного рецидива более чем в 3 раза (относительный риск 0,31; 2p<0,00001), но также и риск смерти от РМЖ на протяжении 15 лет (относительный риск 0,83; 2p=0,0002). Частота местных рецидивов при 10-летнем наблюдении у больных без поражения лимфатических узлов составила 29,2% при отсутствии лучевой терапии и 10,0% – при ее проведении. У больных с поражением лимфатических узлов эти показатели соответствовали 46,5% и 13,1%. 10-летняя смертность от РМЖ у больных без поражения лимфатических узлов составила 20,3% при отсутствии лучевой терапии и 17,4% при проведении лучевой терапии, а у больных с поражением лимфатических узлов – 45,2% и 36,5% соответственно. С другой стороны, проведение лучевой терапии сопровождалось повышением частоты рака легкого в 1,61 раза (2р=0,0007), рака пищевода – в 2,06 раза (2р=0,05), лейкозов – в 1,71 раза (2р=0,04), сарком мягких тканей – в 2,34 раза (2р=0,05), а также повышением смертности от болезней сердца в 1,27 раза (2р=0,0001), от тромбоэмболии легочной артерии – в 1,94 раза (2р=0,02), от рака легкого в – 1,78 раза (2р=0,0004), от рака пищевода – в 2,40 раза (2р=0,04).
Таблица 2. Методы органосохраняющего лечения рака молочной железы.
| Группа больных | Характер органосохраняющего лечения | Число больных | Стадия | 5-летние результаты, % | Местные рецидивы | Отдаленные метастазы | Выживаемость |
|---|---|---|---|---|---|---|---|
| I | Секторальная резекция + Д1 | 2441 | I-IIА Т1-2N0М0 | 7,6-40,4 | 10,1 | 92,8 | |
| II | Туморэктомия или секторальная резекция + ЛТ | 3478 | I-IIА Т1-2N0М0 | 7,1-13,5 | 10,5 | 91,8 | |
| III | Туморэктомия или секторальная резекция с Д1 + ЛТ | 6560 | I-IIА Т1-2N0М0 (опухоль до 4 см) | 6,2-10,2 | 7,8 | 87,3 | |
| IV | Радикальная резекция | 286 | I-IIА Т1-2N0М0 | 4,6-9,1 | 8,7 | 89,4 | |
| V | Радикальная резекция + ЛТ | 800 | I-IIА Т1-2N0М0 | 4,2-4,6 | 9,2 | 92,6 | |
| ВСЕГО | 13785 | ||||||
Для больных I группы показатель общей выживаемости составил 92,8%, II группы – 91,8%, III группы – 87,3%, IY группы – 89,4%, V группы – 92,6%. Достоверно чаще местные рецидивы встречались в I группе больных, у которых органосохраняющие операции выполнены без удаления лимфатических узлов регионарных зон и дополнительной лучевой терапии. Частота местных рецидивов в среднем составила 28,6%. Среди больных, получавших дополнительное лечение, в послеоперационном периоде этот показатель был примерно в 3-4 раза меньше и составил от 8,4% до 2,4%. Приведенные данные позволяют сделать вывод, что лучевая терапия после органосохраняющих операций достоверно снижает частоту местных рецидивов рака. Отдаленные метастазы РМЖ I-IIА стадии во всех группах наблюдали примерно одинаково, независимо от методов органосохраняющего лечения.
Принципиальным в выборе пациенток для органосохраняющих операций является стадия опухолевого процесса. Однако стадия рака, учитывающая в основном количественную характеристику опухолевого процесса и его распространенность, не отражает другие весьма важные стороны заболевания: биологическую и митотическую активность опухоли, темп ее роста, гетерогенность опухолевых клеток, реактивность организма и гормонального статуса, что в конечном итоге определяет прогноз заболевания. Хирургическое вмешательство должно быть одновременно радикальным и абластичным, но в то же время преследовать задачу ранней реабилитации. Поэтому при выполнении органосохраняющих операций необходимо стараться сохранить форму молочной железы, тем самым уже на хирургическом этапе решая задачу улучшения качества жизни больных.
Остановимся на особенностях возникновения местного рецидива РМЖ. При анализе результатов органосохраняющих операций неизбежно возникает вопрос: действительно ли развитие местного рецидива в молочной железе не приводит к повышению риска диссеминации процесса и ухудшению общей выживаемости?
Одни авторы считают рецидив только местным процессом, при возникновении которого своевременно выполненная мастэктомия или удаление рецидива с повторным облучением решают проблему для большинства больных. В результате показатели общей выживаемости групп пациенток статистически значимо не различались.
Другие считают, что возникновение рецидива предшествует генерализации онкологического процесса, исходя из того, что рецидивная опухоль является источником диссеминации или к началу лечения болезнь была уже распространенной, а местный рецидив явился маркером активации опухолевого процесса.
Возможна двоякая трактовка этих результатов: а) рецидивная опухоль является источником диссеминации опухоли; б) к началу лечения болезнь уже была диссеминирована, местный рецидив является только маркером активности опухолевого процесса, следовательно, объем операции, проведение лучевой терапии не имеют значения для выживаемости больных.
Как писали B. Fisher и соавт. (1991), «связь между местным рецидивом и отдаленным метастазированием не является причинной. Отдаленные метастазы возникают с равной частотой как у больных с органосохраняющей операцией, так и с мастэктомией. Местный рецидив – предсказатель риска, а не причина отдаленных метастазов».
Еще один негативный фактор при органосохраняющих операциях – наличие опухолевых клеток в перитуморальных сосудах. Данный фактор напрямую связан с отдаленным метастазированием и при отсутствии адъювантной химиотерапии повышает вероятность развития отдаленных метастазов у больных, независимо от объема оперативного пособия на молочной железе.
При инвазивном протоковом раке частота раковой эмболии в кровеносных сосудах колеблется от 21% до 75%, экстратуморальную эмболию выявляют в 25%, при этом у 91-100% этих больных наблюдается метастатическое поражение лимфатических узлов. Одни авторы считают инвазию кровеносных сосудов плохим прогностическим признаком только при поражении двух и более лимфатических узлов. Другие полагают, что прогностическое значение этого признака играет роль только при отсутствии метастазов в лимфатических узлах, когда риск рецидива у больных с инвазией сосудов в ткани железы в 4,7 раза выше по сравнению с группой больных с отсутствием данного признака. При инвазии сосудов в ткани железы частота рецидивов составляет от 14; до 29,5%.
Основным методом борьбы с рецидивами является лучевая терапия.
По данным ЕSMO, послеоперационная лучевая терапия рекомендуется всем больным, перенесшим органосохраняющие операции. Облучение всей молочной железы снижает риск развития местного рецидива на 2/3, а подведение дополнительного буста снижает его еще на 50%. Кроме того, лучевая терапия оказывает положительное влияние на выживаемость. В целом, облучение бустами показано и пожилым больным, но может не проводиться при сочетании факторов низкого риска местного рецидива (широкие края резекции, N0, отсутствие сосудистой инвазии). У больных старше 70 лет с гормонозависимыми опухолями, максимальной стадией рТ1N0 и негативными краями резекции возможен отказ от лучевой терапии без ущерба выживаемости. Частичное облучение молочной железы вне рамок клинического исследования не рекомендуют.
При органосохраняющих операциях облучают молочную железу РОД 1,8-2 Гр до СОД 45-50 Гр, при подведении буста доза обычно составляет 10-16 Гр фракциями по 2 Гр, регионарные зоны облучают при медиальной локализации опухоли (облучение парастернальных лимфатических узлов РОД 2 Гр до СОД 46 Гр). При поражении лимфатических узлов облучают зоны регионарного метастазирования РОД 2 Гр до СОД 46 Гр.
Возможны более короткие схемы фракционирования (16 фракций по 2,66 Гр), которые обладают примерно такой же эффективностью и сопоставимыми побочными эффектами, но должны использоваться с осторожностью у молодых пациенток или после дополнительного облучения регионарных зон, т.к. эти категории больных либо вовсе не оценены в соответствующих клинических исследованиях, либо их количество было минимальным. При отказе от облучения после экономных операций локальный рецидив развивается у 15-40% больных.
Однако в 2010 г. канадские исследователи пришли к выводу, что при раннем раке молочной железы 3-недельный курс облучения более высокими дозами столь же эффективен, как и стандартная 5-недельная лучевая терапия. 10-летний риск локального рецидива у 662 женщин, получивших короткий курс облучения, составил 6,2% против 6,7% у 612 женщин после стандартной лучевой терапии. Кроме того, хороший косметический эффект через 10 лет отмечен у 71,3% пациенток, прошедших стандартное облучение, и у 69,8% женщин, получивших укороченный курс.
В НИИ онкологии им. Н.Н. Петрова проведено рандомизированное исследование по оценке эффективности послеоперационной лучевой терапии инвазивного протокового рака молочной железы рТ1-2N0M0 у 317 больных с размерами опухоли до 2,5 см включительно. У подавляющего большинства пациенток (240 из 317) хирургическое вмешательство выполняли в объеме широкой секторальной резекции (77 женщин из 317) или сегментарной резекции, дополненной аксиллярной диссекцией II уровня. Наряду с лучевым лечением больные получали химиотерапию и гормонотерапию.
Лучевую терапию получали 149 женщин, из них у 80 облучена только оставшаяся молочная железа в СОД 50-60 Гр (РОД 2 Гр × 5 раз в неделю), а у 69 лучевому воздействию (СОД 40-50 Гр, РОД 2 Гр × 5 раз в неделю) подвергались и зоны регионарного метастазирования.
В данном исследовании основным фактором, определяющим влияние облучения на отдаленные результаты лечения, оказалась величина опухоли. Как видно из таблицы 2, 5-летняя частота рецидивов при размерах опухоли менее 1 см статистически не различалась и в группе женщин, подвергнутых лучевой терапии, и среди тех, кто ее не получал.
Таблица 3. Частота рецидивов рака молочной железы у больных с размером опухоли <1 см (n=91).
| Тип рецидива | Контроль | Лучевая терапия | р |
|---|---|---|---|
| Рецидив в послеоперационном рубце | 0/51 | 1/40 (2,5%) | >0,05 |
| Рецидив в другом квадранте | 3/51 (5,9%) | 2/40 (5%) | >0,05 |
| Рецидив в молочной железе | 3/51 (5,9%) | 3/40 (7,5%) | >0,05 |
| Рецидив в регионарных лимфатических узлах | 2/51 (3,9%) | 2/40 (5%) | >0,05 |
| Местно-регионарный рецидив | 5/51 (9,8%) | 5/40 (12,5%) | >0,05 |
Совершенно иная картина наблюдалась у больных с опухолями от 1 до 2,5 см включительно. У них послеоперационная лучевая терапия способствовала отчетливому сокращению числа местно-регионарных рецидивов с 9,4% до 1,8% и достоверному (р<0,05) повышению 5-летней безрецидивной выживаемости с 91,0±4,1 до 97,8±1,6% (табл. 4).
Таблица 4. Частота возникновения рецидивов рака молочной железы
у больных с размером опухоли от 1 до 2,5 см включительно (n=226).
| Тип рецидива | Контроль | Лучевая терапия | р |
|---|---|---|---|
| Рецидив в послеоперационном рубце | 3/117 (2,6%) | 1/109 (0,9%) | >0,05 |
| Рецидив в другом квадранте | 5/117 (4,3%) | 0/109 | <0,05 |
| Рецидив в молочной железе | 8/117 (6,8%) | 1/109 (0,9%) | <0,05 |
| Рецидив в регионарных лимфатических узлах | 3/117 (2,6%) | 1/109 (0,9%) | >0,05 |
| Местно-регионарный рецидив | 11/117 (9,4%) | 2/109 (1,8%) | <0,05 |
Исходя из полученных данных, радиационное воздействие на молочную железу, включая зоны регионарного метастазирования или без них, у больных РМЖ рТ1N0М0 с размером опухоли 1 см и менее не способствует снижению частоты местного рецидива. В то же время при опухолях более 1 см, но не превышающих 2,5 см (рТ1-2N0М0), облучение приводит к достоверному (р<0,05) уменьшению процента местно-регионарных рецидивов и соответствующему увеличению безрецидивной выживаемости.
Материалы и методы
В отделении общей онкологии МНИОИ им. П.А. Герцена с 2000 по 2006 гг. выполнено 438 радикальных резекций с/без пластики молочной железы. Общее число больных – 435, у 3 пациенток диагностирован первично-множественный синхронный рак молочных желез, во всех 3 случаях была выполнена двусторонняя радикальная резекция. Распределение пациенток по стадиям: 0 – 5 (1,1%), I – 181 (41,3%), IIА – 154 (35,3%), IIБ – 44 (10%), IIIА – 51 (11,6%), IIIВ – 1 (0,2%), IIIС – 2 (0,5%).
Мультицентричный первично-множественный рак в виде нескольких очагов опухоли в одной молочной железе наблюдали у 51 (11,6%) пациентки.
Лучевую терапию проводили у 296 (67,6%) больных.
По стандартам лечения с учетом показаний проводили курсы полихимиотерапии по схемам CAF, АС, ТАС, АТ. Число курсов полихимиотерапии составило 4-6.
В случае гормонопозитивной опухоли назначали гормонотерапию: женщинам с сохраненной менструальной функцией – антиэстрогены до 5 лет, как с выключением, так и без выключения функции яичников. На современном этапе выключение функции яичников осуществляют с помощью гормонов (золадекс) или лапароскопического удаления яичников. При приеме тамоксифена контролируют органы мишени (матка) с помощью ультразвукового исследования для исключения гиперплазий и других новообразований эндометрия.
В случае менопаузы предпочтение отдают ингибиторам ароматазы с тем же периодом назначения до 5 лет. При необходимости корригируют возможные побочные эффекты назначаемых препаратов, а именно – остеопороз.
При экспрессии рецепторов Неr2/neu 3+ назначают таргетную терапию по показаниям – герцептин, лапатиниб до 6 мес. приема.
Мы проанализировали рецидивы в оставшейся части молочной железы у 435 больных. За 5 летний срок наблюдения диагностировано 10 (2,3%) рецидивов. До 10-летнего срока наблюдения рецидивы диагностированы в 20 (4,6%) случаях.
С целью обнаружения местных рецидивов выполняли клиническое обследование, ультразвуковое исследование и маммографию.
Традиционно под рецидивами РМЖ подразумевают возобновление опухолевого роста в молочной железе и в зонах расположения регионарных лимфатических узлов. Нередко указывают на характер роста рецидива: одиночный или множественный, узловой или диффузный (он же – лимфангитический, инфильтративный, панцирный).
Сроки возникновения рецидива составили от 1,5 до 11 лет (табл. 5). У одной больной в оставшейся части молочной железы в области сосково-ареолярного комплекса выявлен рак Педжета, еще у одной в дальнейшем возникла карциносаркома. Одномоментное появление рецидива и отдаленных метастазов диагностировано у 6 пациенток.
Таблица 5. Время возникновения рецидивов.
| Время возникновения рецидивов | Число рецидивов |
|---|---|
| До 3 лет | 3 |
| 3-5 лет | 7 |
| 5-11 лет | 10 |
| Всего | 20 |
Изучение зависимости возникновения рецидива от гистогенеза опухоли выявило следующую картину: инвазивный протоковый рак II степени злокачественности – 8, инвазивный протоковый рак III степени злокачественности – 5, комбинированный рак – 2, инвазивный дольковый рак – 2, рак Педжета – 1, слизистый рак – 1, без гистологического определения (IY степень лечебного патоморфоза) – 1 (табл. 6). В 4 случаях неблагоприятными морфологическими признаками прогноза возникновения рецидива были раковые эмболы в сосудах вблизи опухолевого узла, рост инвазивного рака, c-r in situ вблизи опухолевого узла.
Таблица 6. Зависимость частоты рецидивов РМЖ от гистологической формы опухоли.
| Гистологическая форма рака | Число больных | Рецидивы | |
|---|---|---|---|
| абс. | % | ||
| Инвазивный протоковый II степени злокачественности | 214 | 8 | 3,8 |
| Инвазивный протоковый III степени злокачественности | 76 | 5 | 6,6 |
| Инвазивный дольковый | 50 | 2 | 4,0 |
| Инвазивный дольковый в комбинации с инвазивным протоковым | 43 | 2 | 4,6 |
| Другие формы | 55 | 3 | 5,4 |
| Всего | 438 | 20 | 4,6 |
Таблица 7. Рецидивы РМЖ в оставшейся части молочной железы
в зависимости от стадии у больных, не получавших лучевую терапию.
| Стадии РМЖ | Число пациенток | Число рецидивов |
|---|---|---|
| I (Т1N0М0) | 108 | 4 (3,7%) |
| IIА (Т2N0М0, Т1N1М0) | 27 | 4 (14,8%) |
| IIБ (Т2N1М0) | 1 | 1 (100%) |
| Всего | 136 | 9 (6,6%) |
Таблица 8. Рецидивы РМЖ в оставшейся части молочной железы
в зависимости от стадии у больных, получавших лучевую терапию.
| Стадии РМЖ | Число пациенток | Число рецидивов |
|---|---|---|
| I (Т1N0М0) | 73 | 3 (4,1%) |
| IIА (Т2N0М0, Т1N1М0) | 127 | 2 (1,6%) |
| IIБ (Т2N1М0) | 43 | 1 (2,3%) |
| III А (Т1-3N1-2М0) | 50 | 5 (10%) |
| Всего | 293 | 11 (3,8%) |
Самый высокий процент рецидива выявлен при НЕR2-подтипе РМЖ (10%), на 2 месте – трижды-негативный РМЖ (6,1%), на 3 месте – люминальный А подтип (3,1%).
Лечение рецидивов заключалось в следующем: удаление оставшейся части молочной железы – у 14 пациенток, их которых у 5 удаление молочной железы дополнено интраоперационной ФДТ, у 5 – подкожное удаление молочной железы с одномоментной реконструкцией, что связано с возможностью данного вмешательства. Одной пациентке из-за множественных отдаленных метастазов проведена полихимиотерапия.
Таким образом, у 25% больных удалось сохранить молочную железу, увеличив объем операции до подкожной мастэктомии с первичной пластикой аутотканями или в комбинации с эндопротезами. В последующем в данной подгруппе рецидивов не выявлено.
В 4 наблюдениях рецидивы возникли у женщин молодого возраста (до 40 лет), в 16 – после 40 лет (женщин до 40 лет – 34, после 40 лет – 401), т.е. у женщин молодого возраста риск возникновения рецидива высок (11,8%), у женщин более старшего возраста он ниже (3,9%; р<0,05).
Заключение
С учетом новых данных о подтипах РМЖ и результатов нашего исследования можно рекомендовать не выполнять лучевую терапию после органосохраняющих операций при узловых образованиях 1 см и меньше и при благоприятных морфологических критериях (отсутствие мультицентричности, раковых эмболов по периферии узла и в ткани молочной железы, отсутствие инвазивного протокового рака III степени злокачественности, а также трижды-негативного и НЕR2 подтипа РМЖ).
За 5 лет наблюдений за больными РМЖ, перенесшими органосохраняющее лечение, рецидивы развились у 10 (2,3%) пациенток.
Таким образом, на частоту появления рецидивов влияет стадия РМЖ, молодой возраст пациенток, гистогенез и подтип опухоли. При сочетании неблагоприятных прогностических факторов следует прибегать к реоперации на молочной железе.
Послеоперационное облучение оставшейся части молочной железы не оказало достоверного влияния на частоту рецидива, но время до его возникновения увеличилось на 3-4 года.
При наличии неблагоприятных прогностических факторов лечение должно быть комбинированным и включать все обязательные компоненты для снижения риска рецидивов и отдаленных метастазов.
Несомненно, число органосохраняющих операций должно быть увеличено за счет улучшения диагностики и, как следствие, выявления начальных стадий РМЖ. Выполнять пациенткам при РМЖ I стадии калечащую мастэктомию, когда можно выполнить радикальную резекцию молочной железы, наверное, слишком радикальный метод хирургического лечения.
Выполнение экономных органосохраняющих операций (лампэктомия, туморэктомия) на молочной железе и на лимфатических путях (Д1) возможно только у ограниченного числа больных при I стадии РМЖ и небольшом размере опухолевого узла, поскольку расширение показаний для данных операций приведет к высокому проценту рецидивов, а также увеличению риска появления отдаленных метастазов, и, соответственно, необходимости повторной операции и комплексного лечения.
Литература
- Берштейн Л.М., Семиглазов В.Ф. Подтипы рака молочной железы и их гормонально-метаболическое «обеспечение»: прикладной аспект. VIII Международная ежегодная конференция «Проблемы диагностики и лечения рака молочной железы». СПб, 2011; 42-52.
- Бурлаков А.С. Радикальность или сохранение органа в хирургическом лечении рака молочной железы: косметика и онкология. Российский онкологический журнал 2002; 2: 8-12.
- Давыдов М.И., Летягин В.П. Практическая маммология. М., 2007; 272 с.
- Дмитриев А.А. Органосохраняющие операции при раке молочной железы: Автореф. дис. канд. мед. наук. СПб, 2001; 24 с.
- Дружков О.Б., Гатауллин И.Г., Дружков Б.К., Дружков М.О. Подкожная радикальная резекция: IX Международный конгресс. Казань, 2009; 79.
- Ермаков А.В. Экономные операции у больных с начальными стадиями рака молочной железы: Автореф. дис. канд. мед. наук. М., 2004; 36 с.
- Канаев С.В. Роль лучевой терапии в лечении рака молочной железы. Практическая онкология 2002; 3(1): 45-51.
- Криворотько П.В., Семиглазов В.В., Канаев С.В. и др. Факторы, влияющие на развитие местного рецидива после органосохраняющих операций на молочной железе: VIII Международная ежегодная конференция «Проблемы диагностики и лечения рака молочной железы». СПб, 2011; 21-31.
- Орлов О.А. Совершенствование ранней диагностики и хирургического этапа органосохраняющего лечения рака молочной железы: Автореф. дис. д-ра мед. наук. Пермь, 2001; 48 с.
- Пак Д.Д. Органосохраняющие, функционально-щадящие и реконструктивно-пластические операции при комбинированном лечении больных раком молочной железы: Дис. д-ра мед. наук. М., 1998; 569 с.
- Пак Д.Д., Рассказова Е.А., Ермощенкова М.В. Рак молочной железы. М., 2010; 160 с.
- Пасов В.В. Особенности клинического течения и методы лечения местных лучевых повреждений у больных раком молочной железы: Автореф. дис. д-ра мед. наук. Обнинск, 2000; 38 с.
- Портной С.М., Лактионов К.П., Коротких И.Ю. Органосохраняющие операции при раке молочной железы. Онкохирургия-2010 «В будущее через новые технологии». М., 2010; 156-157.
- Семиглазов В.В., Семиглазов В.Ф., Ермаченкова А.М. Диагностика и лечение минимальных форм рака молочной железы. VIII Международная ежегодная конференция «Проблемы диагностики и лечения рака молочной железы. СПб, 2011; 144-149.
- Тер-Арутюнянц С.А., Осипов В.В., Аксененко А.В., Полюшкин Д.В. Ускоренное частичное облучение молочной железы в плане комбинированного лечения: альтернатива традиционному курсу дистанционной лучевой терапии? Онкохирургия-2010 «В будущее через новые технологии». М., 2010; 158-159.
- Хмелевский Е.В. Лучевая терапия рецидивов рака молочной железы. Вопр. онкол. 2000; 46(2): 167-171.
- Чиссов В.И., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2009 году (заболеваемость и смертность). М., 2011; 260 с.
- Аspergen К, Holmberg L, Adami H-O. Standardization of the surgical technique in breast-conserving treatment of breast cancer. Br J Surg 1988; 76: 807-810.
- Fisher B, Anderson S, Fisher E, et al. Significance of ipsilateral breast tumour recurrence after lumpectomy. Lancet 1991; 338(8763): 327-331.
- Fisher В, Anderson S, Redmond CK, et al. Reanalysis and results after 12 years of follow-up in a randomized clinical trial comparing total mastectomy with lumpectomy with or without irradiation in the treatment of breast cancer. N Engl J Med 1995; 333: 1456.
- Kris MG, Benowitz SI, Adams S. Успехи клинической онкологии 2010: наиболее значимые достижения в лечении, профилактике и скрининге онкологических заболеваний. Сообщение Американского общества клинической онкологии (ASCO). Журнал клинической онкологии 2011; 5(1): 80-101.